Một hợp chất có phân tử gồm 1 nguyên tử của nguyên tố X liên kết với 2 nguyên tử O và nặng hơn phân tử hiđro là 32 lần.
•a.Tính phân tử khối của hợp chất.
•b. Tính nguyên tử khối của X, cho biết tên và kí hiệu hóa học của nguyên tố đó.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTK của hợp chất nặng hơn phân tử hidro 31 lần
Phân tử khối của phân tử hidro là 1.2 = 2 đvC
⇒ Phân tử khối của hợp chất là: 2.31 = 62 đvC
b. PTK hợp chất = 2.NTK X + 1.NTK O = 62 đvC
⇒ 2.NTK X + 16 = 62 đvC
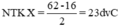
Vậy nguyên tử khối của X là 23. Nguyên tố X là natri (Na)

PTK của hợp chất = $32M_{H_2} = 32.2 = 64(đvC)$
Suy ra : X + 16.2 = 64 $\Rightarrow X = 32$
Vậy X là lưu huỳnh, KHHH : S
PTKhidro = 1.2 = 2
→ PTKh/c = 32.2 = 64
→ NTKX = 64 - 16.2 = 32
→ X là nguyên tố Lưu huỳnh. Kí hiệu là S

a)
$M_{hợp\ chất} = 31.2 = 62(đvC)$
b)
Ta có :
$M_{hợp\ chất} = 2X + 16 = 62 \Rightarrow X = 23(Natri)$
Kí hiệu : Na

gOI HỢP CHẤT là \(XO_2\)
Theo bài: \(M_{XO_2}=32M_{H_2}=64\left(đvC\right)\)
Mà \(M_X+2M_O=64\Rightarrow M_X=32\left(đvC\right)\)
Vậy X là nguyên tố lưu huỳnh.KHHh:S

Bài 11:
a. Gọi CTHH là: XO3
Theo đề, ta có: \(d_{\dfrac{XO_3}{H_2}}=\dfrac{M_{XO_3}}{M_{H_2}}=\dfrac{M_{XO_3}}{2}=56\left(lần\right)\)
=> \(M_{XO_3}=PTK_{XO_3}=112\left(đvC\right)\)
b. Ta có: \(PTK_{XO_3}=NTK_X+16.3=112\left(đvC\right)\)
=> NTKX = 64(đvC)
=> X là đồng (Cu)
c. \(N=\dfrac{26,284}{112}.6,023.10^{23}=1,413469036.10^{23}\)
a)
$PTK = 32M_{H_2} = 32.2 = 64(đvC)$
b)
$X + 16.2 = 64 \Rightarrow X = 32$
Vậy X là lưu huỳnh, KHHH : S