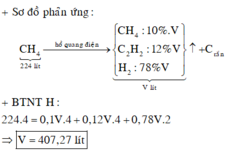
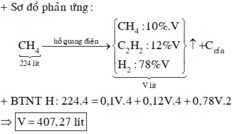
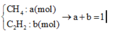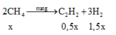Cho 500 m3 metan qua hồ quang (giả sử lúc đó chỉ xảy ra hai phản ứng: 2CH4 ➝ C2H2 + 3H2; CH4 ➝ C + 2H2. Hỗn hợp khí thu được là hỗn hợp A gồm 12% C2H2, 10% CH4, 78% về thể tích. Tính thể tích của hỗn hợp khí A biết các thể tích khí được đo ở đktc? Tính % metan bị phân hủy thành C và % metan bị chuyển hóa thành C2H2? Nếu lấy tất cả lượng C2H2 để điều chế PVC thì thu được bao nhiêu kg biết hiệu suất của quá trình điều chế là 70%
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Những câu hỏi liên quan

23 tháng 10 2017
Đáp án : A
nCH4=10 mol
2CH4 --> C2H2 + 3H2 (1)
2x------->x-------->3x
CH4 -->C + 2H2 (2)
y------------->2y
sau phản ứng ta được:
x(mol) C2H2; 10-(2x+y) (mol) CH4 và 3x+2y (mol) H2
ta có các phương trính sau:
x/0,12 = [10 - (2x + y)]/0,1 = (3x + 2y)/0,78
Giải ra ta được:
x=24/11; y=42/11
Tổng số mol của các khí trong A là:
x+10-(2x+y)+3x+2y=2x+y+10=18,1818 mol
Vậy V=18,1818.22,4 = 407.2727 (l)
NH
1