1 nguyên tử của nguyên tố X có điện tích hạt nhân là 53. Tỉ số nơtron và điện tích hạt nhân là 1,3962. số nơtron trong nguyên tử X gấp 3,7 lần số nơtron trong nguyên tử Y. Khi cho 1,0725g Y tác dụng với lượng dư X thu được 4,565g sản phẩm có công thức là XY. Hãy xác định X và Y là những nguyên tố nào?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Cấu hình electron phân lớp ngoài cùng của nguyên tố X là 5p5
Cấu hình electron của X là 1s22s22p63s23p63d104s24p64d105s25p5 (Z X = 53)
Tỉ lệ số notron và điện tích hạt nhân là 1,3962 → nX = 74 → AX = 74 + 53 = 127
Số notron trong X gấp 3,7 lần số notron trong Y → nY = 20
Phương trình hóa học : X + Y → XY
Bảo toàn khối lượng → mX = 4,565 - 1,0725 = 3,4925 gam
Theo phương trình có
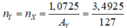
→ AY= 39 → ZY = 39 - 20 = 19
Cấu hình của Y là [Ar]4s1
Số hiệu nguyên tử của X là 53 → A đúng
Y có 4 electron và có 1 electron lớp ngoài cùng → B, C đúng
Số khối của X là 127 → D sai

Đáp án A
Theo giả thiết ta có:
2 Z X + N X = 23 8 Z Y ( 1 ) 2 Z Y + N Y = 16 5 Z X ( 2 ) N X + N Y = 2 Z Y ( 3 )
⇒ - 6 5 Z X + - 7 8 Z Y + N X + N Y = 0 ( 1 ) + ( 2 ) N X + N Y = 2 Z Y ( 3 )
⇔ 9 8 Z X = 6 5 Z X ⇔ Z X Z Y = 15 16

\(\left\{{}\begin{matrix}P=E\\\dfrac{N}{N+P}=\dfrac{11}{20}\\P+E+N=58\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=58\\20N-11N-11P=0\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}2P+N=58\\9N-11P=0\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=Z=18\\N=22\end{matrix}\right.\\ \Rightarrow A=Z+N=18+22=40\left(đ.v.C\right)\\ \Rightarrow KH:^{40}_{18}Ar\)

Chọn C
Điện tích hạt nhân nguyên tử X là 15+ ⇒ X có số p = số e = 15.
Trong nguyên tử X, số hạt mang điện nhiều hơn số hạt không mang điện là 14 nên: (p + e) – n = 14 ⇒ n = (15 + 15) – 14 = 16 → chọn C.
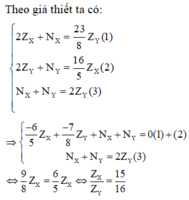

Đặt ZX, NX lần lượt là số proton và notron của nguyên tử X
X có điện tích hạt nhân là 53 => ZX = 53
Có : \(\frac{N_X}{Z_X}=1,3962\Rightarrow N_X=1,3962.Z_X=1,3962.53=74\)
=> Số khối của X là: AX = ZX + NX = 53 + 74 = 127 => X là Iot
\(\text{Có: NY = NX : 3,7 = 74:3,7 = 20 (hạt)}\)
\(\text{X + Y → XY (1)}\)
Bảo toàn khối lượng có: mX + mY = mXY
\(\text{→ mX = 4,565 – 1,0725 = 3,4925 (g)}\)
\(\text{→ nX = mX : MX = 3,4925 : 127 = 0,0275 (mol)}\)
Theo PTHH (1): nY = nX = 0,0275 (mol)
=> MY = mY : nY = 1,0725 : 0,0275 = 39 (g/mol)
=> ZY = MY – NY = 39 – 20 = 19
Y là nguyên tố Kali