Câu 1: Oxi hoá 22,4 gam sắt, thu được 32 gam oxit sắt.
a) Xác định tên và công thức của oxit sắt.
b) Xác định hoá trị của sắt trong oxit này.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Gọi CTHH của oxit sắt là $Fe_2O_n$
$Fe_2O_n + nCO \xrightarrow{t^o} 2Fe +nCO_2$
$n_{Fe} = \dfrac{22,4}{56} = 0,2(mol)$
$\Rightarrow n_{Fe_2O_n} = \dfrac{1}{2}n_{Fe} = 0,2(mol)$
$M_{oxit} = 56.2 + 16n = \dfrac{32}{0,2}=160$
Suy ra : n = 3
Vậy oxit cần tìm là $Fe_2O_3$
b) $n_{CO_2} = \dfrac{3}{2}n_{Fe} = 0,6(mol)$
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
$n_{CaCO_3} = n_{CO_2} = 0,6(mol)$
$m_{CaCO_3} = 0,6.100 = 60(gam)$

Vì sau phản ứng chỉ thu được 1 oxit sắt nên oxit sắt không phải là oxi sắt từ.
Gọi CT oxit là Fe2Oa
Fe2Oa(\(\dfrac{10,8}{112+16a}\))+2aHCl→2FeCla(\(\dfrac{10,8}{56+8a}\))+aH2O
nFe2Oa=\(\dfrac{10,8}{112+16a}\)
⇒\(\dfrac{10,8}{56+8a}.\left(56+35,5a\right)=19,05\)
⇔a=2
Vậy CT của oxit sắt là FeO

a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

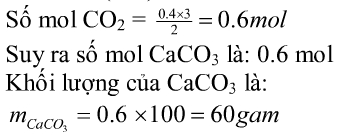
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g

PTPƯ:
FexOy + 2yHCI -------------> xFeCI2y/x +yH2O
1mol ----------------------------> xmol
16/(56x +16y)mol-------------> 32,5/(56 + 71y/x)
=> 16x/(56x + 16y) = 32,5/(56 + 71y/x)
=> 896x +1136y = 1820x + 520y
=>616y = 924x
=> x/y = 2/3
Vậy CT của oxít sắt là Fe2O3
Tham khảo:
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.
Tham khảo
a) Ta có: nFe = 22,4/56 = 0,4 (mol)
2xFe + yO2 −to→ 2FexOy (1)
(mol) 0,4 → 0,4/x
Theo đề bài, ta có phương trình :
0,4/x(56x + 16y) = 32 → 16y = 24x → x/y= 16/24= 2/3
Chọn x=2, y=3 → Công thức oxit sắt : Fe2O3.
b) Hoá trị của sắt trong Fe2O3 là : III.