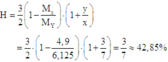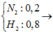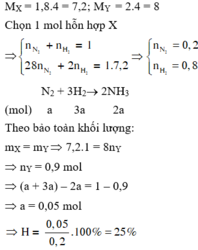Hỗn hợp X có khối lượng 9,28 gam gồm N2, H2( N2 được lấy dư so với H2). Nung nóng X một thời gian trong bình kín có xúc tác thu được hỗn hợp khí Y có tỉ khối so với He là 2,68. Biết hiệu suất của phản ứng tổng hợp NH3 đạt 28%. Thành phần phần trăm về khối lượng của hỗn hợp N2 và H2.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Hỗn hợp ban đầu chứa N 2 : 0 , 2 H 2 : 0 , 8
→ Hiệu suất tính theo N2.
nsau = 3,6/4 = 0,9 → N2 phản ứng = 0,05 → H = 25%

Đáp án B.
Giả sử ban đầu hỗn hợp có 1 mol trong đó có x mol N2 và y mol H2
Ta có x + y =1 mol (1)

Đặt số mol N2 phản ứng là a mol
N2+ 3H2 → 2NH3
Ban đầu 0,2 0,8 mol
Phản ứng a 3a 2a mol
Sau pứ (0,2-a) (0,8-3a) 2a mol


MX = 8,5 . Theo qui tắc đường chéo ta có : 3n N2 = nH2 => Chọn n H2 = 3 mol => n N2 = 1 mol
Xét cân bằng: N2 + 3H2 ó 2NH3
Số mol ban đầu 1 3
Số mol phản ứng x 3x 2x Số mol cân bằng (1-x) (3-3x) 2x Số mol sau phản ứng = (4 – 2x) mol
=>dY/X = nX/nY (do khối lượng chất trong hỗn hợp không đổi)
=> 0,7.4 = 4-2x => x = 0,6 mol
=>H% = 60%
=>D

Đáp án B
Áp dụng phương pháp đường chéo cho hỗn hợp X:
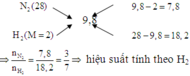
Cách 1: Gọi số mol N2 là 3x thì số mol H2 là 7x ⇒ tổng số mol hỗn hợp X là 3x + 7x = 10x
Thay vào công thức:
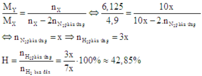
Cách 2: Áp dụng công thức tính nhanh với trường hợp x < 3y:
Hiệu suất phản ứng: