cho 20g hỗn hợp gồm Zn và ZnO tác dụng hết với 100 gam dung dịch HCL thu được 2,24 lít khí ở điều kiện tiêu chuẩn a) viết phương trình hóa học. Tính phần trăm khối lượng mỗi chất trong hỗn hợp. b) Tính nồng độ phần trăm dung dịch muối thu được sau phản ứng. c) nếu cho hỗn hợp tác dụng với H2 SO4 đặc nóng thì thu được bao nhiêu lít khí ở điều kiện tiêu chuẩn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a) \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
b) \(n_{Fe}=n_{H2}=n_{H2SO4}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Al2O3}=15,8-5,6=10,2\left(g\right)\)
c) Ta có : \(n_{Al2O3}=\dfrac{10,2}{102}=0,1\left(mol\right)\Rightarrow n_{H2SO4}=3n_{Al2O3}=0,3\left(mol\right)\)
\(C_{MddH2SO4}=\dfrac{0,1+0,3}{0,2}=2M\)

Đáp án D.
Do H2 chỉ khử được Fe2O3 thành Fe nên B gồm Fe và Al2O3, chỉ có Fe tạo H2
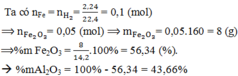

\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.1.......0.2......................0.1\)
Chất rắn X : Cu
\(m_{Zn}=0.1\cdot65=6.5\left(g\right)\Rightarrow m_{Cu}=19.3-6.5=12.8\left(g\right)\)
\(n_{Cu}=\dfrac{12.8}{64}=0.2\left(mol\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
\(2Cu+O_2\underrightarrow{^{^{t^o}}}2CuO\)
\(0.2........0.1\)
\(m_{tăng}=m_{O_2}=0.1\cdot32=3.2\left(g\right)\)

Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{HCl}=2n_{H_2}=0,2\left(mol\right)\Rightarrow C_{M_{HCl}}=\dfrac{0,2}{0,1}=2\left(M\right)\)
\(n_{Fe}=n_{H_2}=0,1\left(mol\right)\Rightarrow m_{Fe}=0,1.56=5,6\left(g\right)\)
\(\Rightarrow m_{Cu}=20-5,6=14,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{5,6}{20}.100\%=28\%\\\%m_{Cu}=72\%\end{matrix}\right.\)

a, \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{10,5}.100\%\approx61,9\%\\\%m_{Cu}\approx38,1\%\end{matrix}\right.\)
c, \(n_{H_2SO_4}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\)

a, Mg + 2HCl \(\rightarrow\) MgCl2 + H2 Cu + 2HCl \(\rightarrow\) CuCl2 + H2
b, \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Cu}=y\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}24x+64y=16\\x+y=\dfrac{2,24}{22,4}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=-0,24\\y=0,34\end{matrix}\right.\)
Xem lại đầu bài nha

a, \(Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
\(ZnO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Zn}=\dfrac{0,1.65}{14,6}.100\%\approx44,52\%\\\%m_{ZnO}\approx55,48\%\end{matrix}\right.\)
c, Ta có: \(n_{ZnO}=\dfrac{14,6-0,1.65}{81}=0,1\left(mol\right)\)
Theo PT: \(n_{CH_3COOH}=2n_{Zn}+2n_{ZnO}=0,4\left(mol\right)\)
PT: \(C_2H_5OH+O_2\underrightarrow{^{mengiam}}CH_3COOH+H_2O\)
Theo PT: \(n_{C_2H_5OH\left(LT\right)}=n_{CH_3COOH}=0,4\left(mol\right)\)
Mà: H = 80%
\(\Rightarrow n_{C_2H_5OH\left(TT\right)}=\dfrac{0,4}{80\%}=0,5\left(mol\right)\)
\(\Rightarrow m_{C_2H_5OH\left(TT\right)}=0,5.46=23\left(g\right)\)
\(\Rightarrow V_{C_2H_5OH}=\dfrac{23}{0,8}=28,75\left(ml\right)\)
\(\Rightarrow V_{C_2H_5OH\left(18,4^o\right)}=\dfrac{28,75}{18,4}.100=156,25\left(ml\right)=0,15625\left(l\right)\)

\(a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ ZnO+2HCl\to ZnCl_2+H_2O\\ b,n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow n_{Zn}=0,15(mol)\Rightarrow m_{Zn}=0,15.65=9,75(g)\\ \Rightarrow \%_{Zn}=\dfrac{9,75}{25,95}.100\%=37,57\%\\ \Rightarrow \%_{ZnO}=(100-37,57)\%=62,43\%\\ c,n_{ZnO}=\dfrac{25,95-9,75}{81}=0,2(mol)\\ \Rightarrow n_{HCl}=2.0,15+2.0,2=0,7(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{0,7.36,5}{12\%}=212,92(g)\)
a) PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
b) Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=n_{Zn}\) \(\Rightarrow n_{ZnO}=\dfrac{20-0,1\cdot65}{81}=\dfrac{1}{6}\left(mol\right)\)
\(\Rightarrow n_{ZnCl_2}=n_{Zn}+n_{ZnO}=\dfrac{4}{15}\left(mol\right)\)
Mặt khác: \(m_{H_2}=0,1\cdot2=0,2\left(g\right)\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=119,8\left(g\right)\) \(\Rightarrow C\%_{ZnCl_2}=\dfrac{\dfrac{4}{15}\cdot136}{119,8}\cdot100\%\approx30,27\%\)
c) Giả sử khí là SO2
PTHH: \(Zn+H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}ZnSO_4+SO_2\uparrow+H_2O\)
Theo PTHH: \(n_{SO_2}=n_{Zn}=0,1\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,1\cdot22,4=2,24\left(l\right)\)