Nếu từ 10 tấn quặng pyrit chứa 60% FeS2 thì có thể sản xuất bao nhiêu kg đ H2SO4 96%
Nếu Hiệu suất chung 40%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Điều chế H2SO4 từ FeS2 qua các dãy biến hóa sau:
FeS2 -> 2SO2 -> 2SO3 -> 2H2SO4
120kg....................................2x98 kg
60kg.....................................98kg
Theo lý thuyết khối lượng H2SO4 sinh ra là 98 kg, nhưng hiệu suất 85% nên thực tế chỉ thu đc:
(98 x 85 ) : 100 = 83,3 kg
Khối lượng dd H2SO4 96% thu đc là:
100 kg dd có 96 kg H2SO4
x kg dd có 83,3 kg
=> x = (83,3 . 100 ) : 96 = 86,77 kg
b) Lượng S trong 80 tấn quặng pirit
(40 . 80) : 100 = 32 tấn
Điều chế H2SO4 từ S qua dãy biến hóa sau:
S -> SO2 -> SO3 -> H2SO4
32 tấn.......................98 tấn
Nếu tính theo lý thuyết ta thu đc 98 tấn H2SO4
Vậy hiệu suất của quá trình là: (92 x 100) : 98 = 93,88 %

Đáp án C.
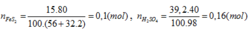
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

4 FeS2 + 11 O2 -to-> 2 Fe2O3 + 8 SO2
5.105<----------------------------------106 (mol)
SO2 + 1/2 O2 -to-> SO3
106<--------------------106 (mol)
SO3 + H2O -> H2SO4
106<---------------106 (mol)
mH2SO4= 98% x 100=98(tấn)
=> nH2SO4= (98.106)/98=106 (mol)
n(FeS2,thực tế)= (5.105): 90%= 5000000/9 (mol)
=> mFeS2(thực tế)= 5000000/9 x 120 = (2.108)/3 (g)
=> m(quặng pirit)= (2.108)/3 : 96% \(\approx\) 69 444 444,444 (g) \(\approx\) 69,44444444 (tấn)

Đổi 1,2 tấn = 1200 kg
Ta có: \(n_{FeS_2}=\dfrac{1200}{120}=10\left(kmol\right)\)
Bảo toàn Lưu huỳnh: \(n_{H_2SO_4\left(lý.thuyết\right)}=2n_{FeS_2}=20\left(kmol\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(thực\right)}=\dfrac{20\cdot98}{50\%}\cdot80\%=3136\left(kg\right)=3,136\left(tấn\right)\)