Các bạn cho mình hỏi
Bột j chứa gần như 90 phần trăm là S ( lưu huỳnh )
MÔN HÓA NHA
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
\(M_{K_2CO_3}=39.2+12+16.3=138\left(dvC\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,52\%\)
\(\%C=\dfrac{12}{138}.100\%=8,69\%\)
\(\%O=100\%-56,52\%-8,69\%=34,79\%\)
Còn lại cậu làm tương tự nhá

\(Đặt:\left\{{}\begin{matrix}n_{Ca}=x\left(mol\right)\\n_{Zn}=y\left(mol\right)\end{matrix}\right.\\ Ca+S-^{t^o}\rightarrow CaS\\ Zn+S-^{t^o}\rightarrow ZnS\\ Tacó:\left\{{}\begin{matrix}40x+65y=22,5\\x+y=\dfrac{12,8}{32}=0,4\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,14\\y=0,26\end{matrix}\right.\\ \Rightarrow\%n_{Ca}=\dfrac{0,14}{0,4}.100=35\%;\%n_{Zn}=65\%\)

-Dùng nam châm để hút Fe,còn lại là hỗn hợp nhôm và lưu huỳnh
- Đốt hỗn hợp trong không khí. Thu khí bay lên.
PTHH: 4Al + 3O2 → 2Al2O3
S + O2 → SO2
Phần chất rắn cho vào khí H2 dư, đốt nóng. Ta thu được sắt nguyên chất:
Fe3O4 + 4H2 → 3Fe +4H2O
- Sục khí SO2 thu được qua dung dịch H2S dư, lọc chất rắn, sấy khô, thu được lưu huỳnh nguyên chất. PTHH: SO2 + 2H2S → 3S + 2H2O
Cách tách này dựa trên tính khử mạnh của hidro sunfua(H2S) ở chương trình lớp 10
Chúc em học tốt!!@

Công thức hóa học: S x O y
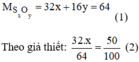
Giải phương trình (2) ta được: x = 1 thay vào pt (1) ⇒ y = 2.
Vậy công thức hóa học của oxit là S O 2

\(PTHH:Fe+S-^{t^o}>FeS\)
BD 0,21875 0,3125
PU 0,21875--> 0,21875---> 0,21875
CL 0----------->0,09375--->0,2175
\(n_{Fe}=\dfrac{m}{M}=\dfrac{14}{64}=0,21875\left(mol\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{10}{32}=0,3125\left(mol\right)\)
\(\dfrac{n_{Fe}}{1}< \dfrac{n_S}{1}\left(\dfrac{0,21875}{1}< \dfrac{0,3125}{1}\right)\)
=> Fe hết , S dư
\(m_S=n\cdot M=\text{0,09375}\cdot32=3\left(g\right)\)
làm lại (suy ngẫm lại thì mik sai)
\(PTHH:Fe+S-^{t^o}>FeS\)
áp dụng ĐLBTKL ta có
\(m_{Fe}+m_S=m_{FeS}\)
\(=>m_S=m_{FeS}-m_{Fe}\\ =>m_S=22-14\\ =>m_S=8\left(g\right)\)
khối lượng lưu huỳnh đã lấy là
\(10-8=2\left(g\right)\)

Bài tập này tuy đơn giản nhưng nếu không hiểu rõ bản chất sẽ dẫn tới đáp án sai. Theo đề bài, hai lưu huỳnh thay thế cho hai hiđro ở nhóm metylen:
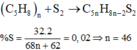
Đáp án C.

a)Phương trình hóa học của phản ứng.
Fe + S -> FeS
xmol xmol
2Al + 3S -> Al2S3.
ymol 1,5y.
b) Tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp ban đầu:
Ta có (mol).
Ta có hệ phương trình :
Giải hệ phương trình được y = 0,02 => mAl = 0,02.27 = 0,54g.
x = 0,01 => mFe =0,01.56 = 0,56 gam.
%mAl = %.
%mFe = 50,91 %.
Theo lượng chất :
%nAl = 66,67%.
%Fe = 33,33%.
)Phương trình hóa học của phản ứng.
Fe + S -> FeS
xmol xmol
2Al + 3S -> Al2S3.
ymol 1,5y.
b) Tỉ lệ phần trăm của sắt và nhôm trong hỗn hợp ban đầu:
Ta có
(mol).
Ta có hệ phương trình :
Giải hệ phương trình được y = 0,02 => mAl = 0,02.27 = 0,54g.
x = 0,01 => mFe =0,01.56 = 0,56 gam.
%mAl =
%.
%mFe = 50,91 %.
Theo lượng chất :
bột lưu hyunh
còn bột j khác ko bạn