Đốt cháy hoàn toàn 9,0 gam hợp chất hữu cơ A (chứa C,H,O) thu được 6,72 lít CO2 (đktc) và 5,4 gam H2O.
a) Tính thành phần trăm của các nguyên tố trong A
b) Lập công thức đơn giản nhất của A
c) Tìm công thức phân tử của X. Biết tỉ khối hơi của X so với khí hidro bằng 1,875

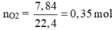
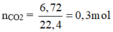
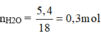
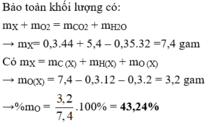
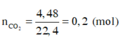
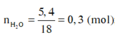
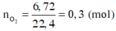
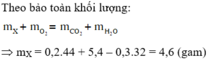
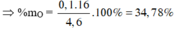
Gọi CTTH của chất hữu cơ A là CxHyOz;
BT C: nC= nCO2=0,3 mol;
BT H : nH= 2nH2O =2* 0,3 =0,6 mol;
%C = 0,3 * 12/9=40%;
% H= 0,6*2 /9=13,33 %;
% O =46,67 %
b,
mA= mC + mH + mO = 9 <--> 0,3* 12 + 0,6* 2 +mO=9;
--> mO =4,2 (g)
--> nO =0,2625 (mol);
Ta có : x:y:z = 0,3 : 0,6 : 0,2625
--> x:y:z = 8: 16 :7 ;
---> C8H16O7;
nCO2= 6.72/22.4=0.3 mol
nC= 0.3 mol
mC= 0.3*12=3.6g
mH2O= 5.4/18=0.3 mol
nH= 0.6 mol
mO= mA - mC - mH= 9 - 3.6 - 0.6=4.8g
nO= 4.8/16=0.3 mol
%C= 3.6/9*100%= 40%
%H= 0.6/9*100%= 6.67%
%O= 4.8/9*100%=53.33%
Gọi CT của A: CxHyOz
x : y : z = 0.3 : 0.6 : 0.3 = 1 : 2 : 1
Vậy: CT đơn giản : CH2O
Mình nghĩ bạn ghi đề sai rồi, phải là tỉ khối so với metan là 1.875
M(CH2O)n= 1.875*16=30
<=> 30n=30
<=> n=1
Vậy: CT của X: CH2O hay HCHO