Bài tập về tính chất của axit H2SO4.
Câu 1 : Hoà tan 5,4 g kim loại X trong dung dịch H2SO4 đậm đặc , đun nóng thu được duy nhất 6,72 L khí SO2 điều kiện chuẩn . Tìm X.
Câu 2 : Hoà tan hết 12,8 g kim loại Cu trong dung dịch H2SO4 đặc , đun nóng , dư thu được duy nhất V L khí SO2 điều kiện chuẩn . Tìm V?
Câu 3 : Hoàn tan hết m g kim loại Mg trong dung dịch H2SO4 đậm đặc , đun nóng thu được duy nhất 11,2 L khí H2S ở điều kiện chuẩn . Tìm m?
Câu 4 : Hoà tan hết m g kim loại Fe trong dung dịch H2SO4 loãng , dư , thu được duy nhất 4,48 L khí ở điều kiện chuẩn . Tìm m và khối lượng muối sau phản ứng?
Câu 5 : Cho 8,8 g hỗn hợp gồm 2 kim loại ở 2 chủ kì kế tiếp thuộc IIA tác dụng với dung dịch H2SO4 loãng dư cho 6,72 L ( đktc ) khí H2 ở điều kiện chuẩn . Hai kim loại đó là :
A. Be - Mg B. Ca - Sr C. Mg - Ca. D.Sr - Ba
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}24x+64y=4,4\\BTe:2x+2y=2n_{SO_2}=2\cdot0,1=0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(m_{Mg}=0,05\cdot24=1,2g\)
\(m_{Cu}=0,05\cdot64=3,2g\)
\(n_{H_2SO_4}=2n_{Mg}+2n_{Cu}=2\cdot0,05+2\cdot0,05=0,2mol\)
\(m_{H_2SO_4}=0,2\cdot98=19,6g\)

Đáp án D
Khi hấp thụ SO2 hết vào dung dịch NaOH thì có thể xảy ra các phản ứng sau:
SO2 + 2NaOH → Na2SO3 + H2O
SO2 + NaOH → NaHSO3
Gọi 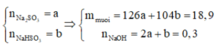
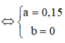
Khi đó
![]()
Gọi n là hóa trị của M.
Áp dụng định luật bảo toàn mol electron, ta có:
Mặt khác
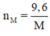 nên
nên 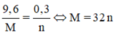
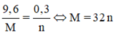
![]()
Là Cu

a)
Gọi $n_{Mg} = a(mol) ; n_{Zn} = b(mol)$
Suy ra: $24a + 65b = 24,3(1)$
$n_{SO_2} = 0,5(mol)$
Bảo toàn electron : $2n_{Mg} + 2n_{Zn} = 2n_{SO_2}$
$\Rightarrow a + b = 0,5(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,3
$m_{Mg} = 0,2.24 = 4,8(gam)$
$m_{Zn} = 0,3.65 = 19,5(gam)$
b)
Ta có :
$n_{H_2SO_4} = 2n_{SO_2} = 1(mol)$
$m_{H_2SO_4\ pư} = 1.98 = 98(gam)$

\(n_{SO_2}=\dfrac{V_{SO_2}}{22,4}=\dfrac{2,24}{22,4}=0,1mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Cu}=y\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=24x\\m_{Cu}=64y\end{matrix}\right.\)
\(Mg+2H_2SO_4\rightarrow MgSO_4+SO_2+2H_2O\)
x 2x x ( mol )
\(Cu+2H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
y 2x y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+64y=4,4\\x+y=0,1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,05.24=1,2g\)
\(\Rightarrow m_{Cu}=0,05.64=3,2\)
\(m_{H_2SO_4}=n_{H_2SO_4}.M_{H_2SO_4}=\left(2.0,05+2.0,05\right).98=0,2.98=19,6g\)
À thêm đk H2SO4 đặc nóng nhá chứ H2SO4 loãng thì PTHH là:
Mg + H2SO4 -> MgSO4 + H2
Cu không tác dụng với H2SO4 loãng

Bài 1 :
\(NaCl + H_2SO_{4_{đặc}} \xrightarrow{t^o} NaHSO_4 + HCl\\ MnO_2 + 4HCl \to MnCl_2 + Cl_2 + 2H_2O\\ Cl_2 + SO_2 + 2H_2O \to 2HCl + H_2SO_4\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O\)

1. X + H2SO4 -> XSO4 +SO2 + H2O
\(n_{so2}\) = \(\frac{6,72}{22,4}\) = 0,3 mol
\(n_{so2}\) = \(n_x\) = 0,3 mol -> \(M_x\) = \(\frac{5,4}{0,3}\) = 18
Xlà Flo
2. Cu + H2SO4 -> CuSO4 + SO2 + 2H2O
\(n_{Cu}\) = \(\frac{12,8}{64}\) = 0,2 mol -> \(n_{SO2}\) = 0,2 mol
\(V_{SO2}\) = 0,2 x 22,4 = 4,48 (l)