Htan htoàn 15,84g hh A gồm Al và Cu bằng dd HNO3 loãng (dư) thu được dd B và 6,272 lít khí NO (sphẩm khử duy nhất ở đktc). Tính % klượng mỗi kim loại trong hhợp A.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Gọi x, y lần lượt là số mol Cu va Fe3O4 phản ứng
=>64x + 232y = 61,2 – 2,4 = 58,8 (1)
Sau phản ứng còn 2,4 gam kim loại đó là Cu, nên trong dung dịch có Cu2+, Fe2+
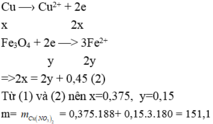

a, \(n_{Cu}=\dfrac{19,2}{64}=0,3\left(mol\right)\)
PTHH: 3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Mol: 0,3 0,8 0,2
\(V_{NO}=0,2.22,4=4,48\left(l\right)\)
b, \(C_{M_{ddHNO_3}}=\dfrac{0,8}{0,4}=2M\)

\(3Ag+4HNO_3\rightarrow3AgNO_3+NO+2H_2O\)
\(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\)
\(NO\) là sản phẩm khử duy nhất.
\(\Rightarrow n_{NO}=\dfrac{0,448}{22,4}=0,02mol\)
Ta có: \(\left\{{}\begin{matrix}27n_{Al}+108n_{Ag}=3,51g\\BTe:3n_{Al}+n_{Ag}=3n_{NO}=0,06\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,01mol\\n_{Ag}=0,03mol\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,01\cdot27}{3,51}\cdot100\%=7,7\%\)
\(\%m_{Ag}=100\%-7,7\%=92,3\%\)

a) \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0,1<----------------------------0,15
=> \(\%m_{Al}=\dfrac{0,1.27}{7,5}.100\%=36\%\)
\(\%m_{Cu}=100\%-36\%=64\%\)
b) \(n_{Cu}=\dfrac{7,5-0,1.27}{64}=0,075\left(mol\right)\)
PTHH: Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
0,075------------------------>0,075
2Al + 6H2SO4 --> Al2(SO4)3 + 3SO2 + 6H2O
0,1----------------------------->0,15
=> VSO2 = (0,075 + 0,15).22,4 = 5,04 (l)

Đáp án A
nNO = 2,8/22,4 = 0,125 (mol)
BTNT N: nNO3 ( trong muối) = 3nNO = 0,375 (mol)
=> mmuối = mKL + mNO3- = 7,55 + 0,375.62 = 30,8 (g)

\(\text{Đ}\text{ặt}:n_{Al}=a\left(mol\right);n_{Cu}=b\left(mol\right)\left(a,b>0\right)\\ Al+6HNO_3\rightarrow Al\left(NO_3\right)_3+3NO_2+3H_2O\\ Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ \Rightarrow\left\{{}\begin{matrix}27a+64b=7,75\\3.22,4a+2.22,4b=7,84\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\\ a,\Rightarrow\%m_{Al}=\dfrac{0,05.27}{7,75}.100\approx17,419\%\\ \Rightarrow\%m_{Cu}\approx82,581\%\\ b,n_{HNO_3}=6a+4b=0,7\left(mol\right)\\ C_{M\text{dd}HNO_3}=\dfrac{0,7}{0,14}=5\left(M\right)\)
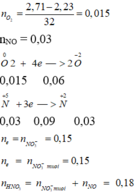
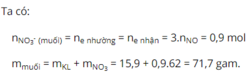
\(n_{NO}=0,28mol\)
\(\left\{{}\begin{matrix}BTe:3n_{Al}+2n_{Cu}=3n_{NO}=0,84\\27n_{Al}+64n_{Cu}=15,84\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,16mol\\n_{Cu}=0,18mol\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,16\cdot27}{15,84}\cdot100=27,27\%\)
\(\Rightarrow\%m_{Cu}=100\%-27,27\%=72,73\%\)