Cho 31,4 ( g ) hỗn hợp Al và Zn tác dụng hết với H2SO4 loãng dư thu được 15,68 (l) H2 (đkc).
a) Tính% khối lượng từng chất trong hỗn hợp ban đầu.
b) Cho hỗn hợp trên tác dụng với H2SO4 đặc , nguội dư. Tính thể tích khí SO2 ( sản phẩm khử duy nhất ) thu được ở đktc?

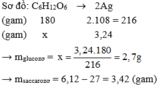
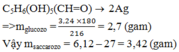

Đặt: nAl= x mol
nZn= y mol
2Al + 3H2SO4 --> Al2(SO4)3 +3H2
x_________________________1.5x
Zn + H2SO4 --> ZnSO4 + H2
y_____________________y
mhh=27x+ 65y= 31.4g (1)
nH2= 1.5x + y = 15.68/22.4=0.7 mol (2)
Giải (1) và (2):
x= 0.2
y=0.4
mAl= 5.4g
mZn= 26g
%Al= 17.97%
%Zn= 82.03%
2Al + 6H2SO4(đ) -to-> Al2(SO4)3 + 3SO2 + 6H2O
0.2_____________________________0.3
Zn + 2H2SO4(đ) -to-> ZnSO4 + SO2 + H2O
0.4_________________________0.4
nSO2= 0.3+0.4=0.7 mol
VSO2= 15.68l