Thực tế khoáng pirit có thể coi là hỗn hợp của FeS2 và FeS. Khi xử lí một mẫu khoáng pirit bằng brom trong dung dịch KOH dư, người ta thu được kết tủa nâu đỏ A và dung dịch B. Nung kết tủa A đến khối lượng không đổi được 0,2 gam chất rắn X. Thêm dung dịch BaCl2 dư vào dung dịch B thu được 1,1087 gam kết tủa trắng Y. Tìm X, X, Y và viết các phản ứng xáy ra ?. Tính khối lượng FeS2 và FeS trong hỗn hợp.

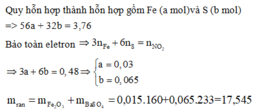


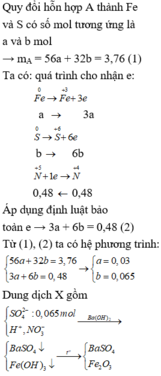


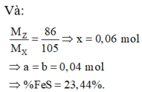
Mình chỉ biết phương trình phản ứng thôi ( thông cảm nha )
Phương trình phản ứng :
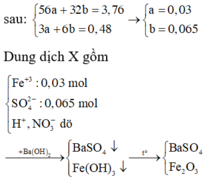
2FeS2 + 15Br2 + 38OH- \(\rightarrow\) 2Fe(OH)3 + 4SO2-4 + 30Br- + 16H2O (1)
2FeS + 9Br2 + 22OH- \(\rightarrow\) 2Fe(OH)3 + 2SO2-4 + 18Br- + 8H2O (2)
2Fe(OH)3 \(\rightarrow\) Fe2O3 + 3H2O (3)
Ba2+ SO-24 \(\rightarrow\) BaSO4 (4)
Bạn phía kia viết pt r nên mk k viết nữa
Gọi: nFeS2=a
nFeS=b
nFe2O3=0,2/160=1.25.10^(-3)
nBaSO4~4,76.10^(-3)
Ta có hệ:
\(\left\{{}\begin{matrix}a+b=2.1,25.10^{-3}\left(BtFe\right)\\2a+b=4,76.10^{-3}\left(BtS\right)\end{matrix}\right.\)
=>a,b
Số hơi kinh khủng nên mừn hăm viết ra đâu ạ =)))