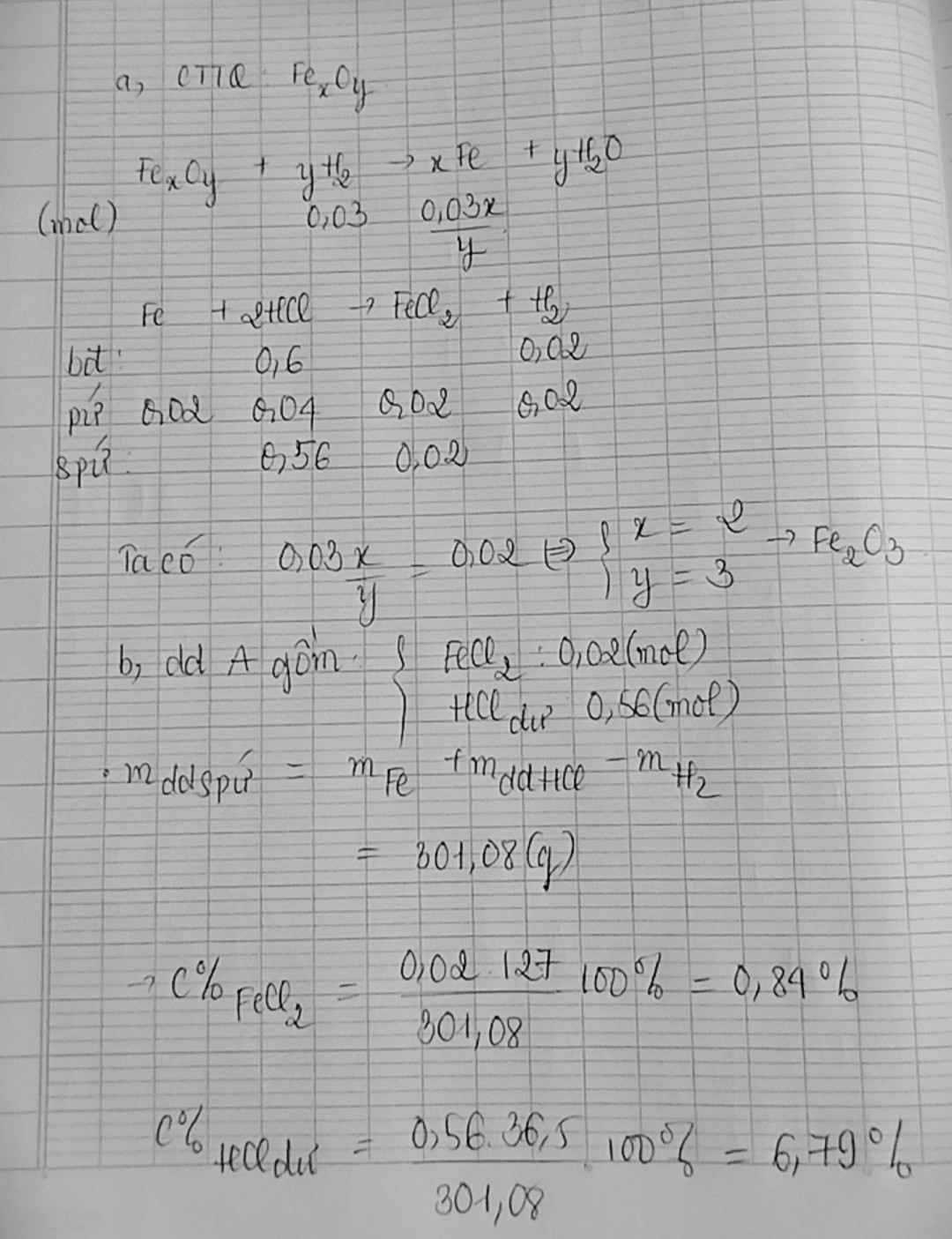dùng H2 dư để khử hoàn toàn m gam bột sắt oxit, thu đc 5,4g nước.hòa tan toàn bộ lượng sắt thu được ở trên bằng dung dịch HCl dư thì thu được 25,4 gam muối. Tìm công thức của oxit sắt??tính giá trị của m??
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{FeCl_2}=\dfrac{25.4}{127}=0.2\left(mol\right)\)
\(n_{H_2O}=\dfrac{5.4}{18}=0.3\left(mol\right)\)
\(Fe_xO_y+yH_2\underrightarrow{t^0}xFe+yH_2O\)
...........................\(x\) ..........\(y\)
...........................\(0.2\) ......\(0.3\)
\(\Rightarrow0.3x=0.2y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{0.2}{0.3}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
\(m_{Fe_2O_3}=0.2\cdot2\cdot160=64\left(g\right)\)

\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\)
Bảo toàn O: \(n_{O\left(oxit\right)}=n_{H_2O}=0,3\left(mol\right)\)
\(n_{FeCl_2}=\dfrac{25,4}{127}=0,2\left(mol\right)\)
PTHH: Fe + 2HCl ---> FeCl2 + H2
0,2 <-------------- 0,2
CTHH của oxit FexOy
=> x : y = 0,2 : 0,3 = 2 : 3
CTHH Fe2O3

Gọi công thức hóa học của oxit sắt là FexOy
PTHH FexOy + y H2 ---> xFe + yH2O (1)
PTHH Fe + 2HCl ---> FeCl2 + H2(khí) (2)
Có n FeCl2 =25,4/127=0,2 (mol)
Từ (2) => n Fe = n FeCl2 = 0,2 (mol)
Từ (1) => n FexOy = \(\dfrac{n_{ }Fe}{x}\) = 0,2/x (mol) (*)
Có n H2O= 5,4/18=0,3 (mol)
Từ (1) => n FexOy = \(\dfrac{nH_2O}{y}\) = 0,3/y (mol) (**)
Từ (*) và (**) => \(\dfrac{0,2}{x}=\dfrac{0,3}{y}\) => x/y = 2/3
Vậy CTHH của oxit sắt là Fe2O3
Có n Fe2O3 = 0,3/y=0,3/3=0,1 (mol)
=> m Fe2O3 = 0,1.160=16 (g)

a, Ta có: \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
___0,1_________________0,1 (mol)
Ta có: \(V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{Fe}=\dfrac{1}{15}.56\approx3,73\left(g\right)\)
Bạn tham khảo nhé!

\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)

n(H2)=1,68/22=0,075m0l
n(CaC03)=10/1O0=0,1m0l
gọi công thức oxit sát là FexOy
Ptpu:
Fex0y + yCO ===> xFe + yC02 (1)
Fe + 2HCL ===> FeCl2 + H2
0,075m0l <-----. . . . . . . . . . ---- 0,075m0l
C02 + Ca(0H)2 ===> CaC03 + H20
0,1m0l <-----. . . . . . . . . . 0,1m0l
Theo tỉ lệ số mol theo phương trình (1) ta co:
x/y=n(Fe)/n(C02)=0,075/0,1=3/4
Vay oxit sat can tim la oxit sat tu Fe304
Than yC02
0,15/x(m0l) <=== 0,15
Theobài thì khối lượng oxit sắt oh 2 p/u = nhau nên số mol = nhau hay (0,225/y)=(0,15/x)
<=>0,225x=0,15y
<=>x=2y/3
<=>x/y=2/3
Vậy oxit có công thức là Fe203

Oxit sắt : FexOy
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} =\dfrac{22,5}{100} = 0,225(mol)\\ Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2\\ n_{oxit} = \dfrac{n_{CO_2}}{y} = \dfrac{0,225}{y}(mol)\\ \Rightarrow \dfrac{0,225}{y}(56x + 16y) = 12\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Vậy CTHH của oxit : Fe2O3

\(P2:\)
\(n_{Fe}=\dfrac{8.4}{56}=0.15\left(mol\right)\)
\(Fe_xO_y+yCO\underrightarrow{^{^{t^0}}}xFe+yCO_2\)
\(\dfrac{0.15}{x}..............0.15\)
\(P1:\)
\(n_{HCl}=0.15\cdot3=0.45\left(mol\right)\)
\(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2\)
\(\dfrac{0.225}{y}.......0.45\)
\(\Rightarrow\dfrac{0.15}{x}=\dfrac{0.225}{y}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0.15}{0.225}=\dfrac{2}{3}\)
\(CT:Fe_2O_3\)
Tại mới lớp 8 nên anh giải hơi chi tiết á :))