Khử 32g Fe2O3 bằng khí H2 dư sau phản ứng thu được m g hỗn hợp chất rắn A. Hòa tan hoàn toàn A bằng dung dịch HCl dư thì thu được 6,72 lít khí ở điều kiện tiêu chuẩn
a. Tính m
b. Tính hiệu suất của phản ứng khử Fe2O3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{21,6}.100\%\approx25,93\%\\\%m_{Fe_2O_3}\approx100-25,93=74,07\%\end{matrix}\right.\)

Đáp án D.
Do H2 chỉ khử được Fe2O3 thành Fe nên B gồm Fe và Al2O3, chỉ có Fe tạo H2
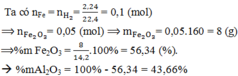
a) mFe2O3=32g->nFe2O3=0.2mol
Fe2O3 + 3H2-> 2Fe + 3H2O
1 : 3 : 2 : 3
0.2 -> 0.6 -> 0.4 -> 0.6
mFe= 0.4*56=22.4g
b) vH2= 6.72-> nH2= 0.3
Fe + 2HCl -> FeCl2 + H2
1 2 1 1
0.3 <- 0.6 <- 0.3 <- 0.3
H= \(\frac{0.3\cdot100}{0.4}\)=75%