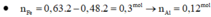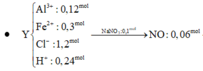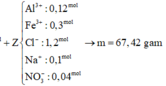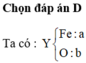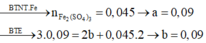Cho m (g) muối halogen của một kim loại kiềm phản ứng với 200 ml dung dịch axít H2SO4 đặc, nóng (lấy dư). Sau khi phản ứng xảy ra hoàn toàn thu được khí X và hỗn hợp sản phẩm Y. Dẫn khí X qua dung dịch Pb(NO3)2 thu được 23,9 (g) kết tủa mầu đen. Làm bay hơi nước cẩn thận hỗn hợp sản phẩm Y thu được 171,2 (g) chất rắn A. Nung A đến khối lượng không đổi thu được muối duy nhất B có khối lượng 69,6(g). Nếu cho dung dịch BaCl2 lấy dư vào Y thì thu được kết tủa Z có khối lượng gấp 1 ,674 lần khối lượng muối B.
1/ Tính nồng độ mol/1ít của dung dịch H2SO4 và m (g) muối.
2/ Xác định kim loại kiềm và halogen.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
a) Khí B mùi trứng thối => H2S
$Pb(NO_3)_2 + H_2S \to PbS + 2HNO_3$
n H2S = n PbS = 47,8/239 = 0,2(mol)
Gọi CTHH của muối halogen là RX
8RX + 5H2SO4 đặc,nóng → 4R2SO4 + H2S + 4X2 + 4H2O
n H2SO4 = 5n H2S = 0,2.5 = 1(mol)
CM H2SO4 = 1/0,2 = 5M
T gồm R2SO4,X2
Khi nung thì chỉ còn lại R2SO4
=> m X2 = 342,4 - 139,2 = 203,2(gam)
n X2 = 4n H2S = 0,8(mol)
=> M X2 = 2X = 203,2/0,8 = 254
=> X = 127(Iot)
Theo PTHH :
n R2SO4 = n X2 = 0,8(mol)
=> M R2SO4 = 2R + 96 = 139,2/0,8 = 174
=> R = 39(Kali)
Vậy Muối cần tìm là $KI$
n KI = 2n R2SO4 = 1,6(mol)
=> x = 1,6.166 = 265,6 gam

Đáp án A
Quy hỗn hợp X chứa hai chất: FeO xmol và Fe2O3 y mol
Cho X+ khí CO→Chất rắn Y + khí Z chứa CO, CO2
CO2+ Ca(OH)2 → CaCO3+ H2O
Có: nCO2= nCaCO3= 0,04 mol
Cho Y + H2SO4 đặc nóng dư thu được nSO2=0,045 mol
- Quá trình cho e:
FeO → Fe3++ 1e
x x mol
C+2 → C+4+ 2e
0,04 0,08 mol
- Quá trình nhận electron:
S+6+ 2e → SO2
0,09← 0,045 mol
Theo định luật bảo toàn electron:
ne cho= ne nhận → x+0,08 = 0,09→ x= 0,01mol
Muối thu được sau phản ứng là Fe2(SO4)3
→ nFe2(SO4)3= 18/400= 0,045 mol
Bảo toàn nguyên tố Fe ta có:
x+ 2y= 0,045.2→ y= 0,04 mol
→ m= mFeO + mFe2O3=72x + 160y= 72.0,01+ 160.0,04= 7,12 gam

Đáp án D
nNaOH = 0,4 (mol)
E + NaOH → 3 muối + khí Z
=> Y C4H12O2N2 phải là muối của Glyxin hoặc Alanin với amin
Gọi CT khí Z: Cn H2n+3N: x (mol) + O2 → 0,25 nH2O + 0,15 ∑ n(CO2 +N2 )
n
H
2
O
Σ
n
(
C
O
2
+
N
2
)
=
(
n
+
1
,
5
)
x
n
x
+
0
,
5
x
=
0
,
25
0
,
15
=
>
n
=
1
=> CTCTcủa Y: CH3-CH(NH2)- COONH3CH3: 0,1 (mol) ( = nNH3 sinh ra)
Gly – Ala – Lys: a mol
Ta có: nNaOH = 3a + 0,1 = 0,4 => a = 0,1
E + HCl
Gly – Ala – Lys + 2H2O + 4HCl → muối
CH3-CH(NH2)- COONH3CH3 + HCl → muối
=> mmuối = 260. 0,1 + 0,2. 18 + 0,4. 36,5 + 0,1.160 + 0,1. 36,5 = 62,25 (g)
Đáp án D
Chú ý:
Lys có 2 nhóm –NH2 trong phân tử do đó 1 mol Gly – Ala – Lys cộng tối đa với 4 mol HCl

Đáp án C
Đặt số mol của M2CO3, MHCO3, MCl là x,y,z mol
Đun nóng X :
2MHCO3 → M2CO3 + H2O + CO2
mrắn giảm = 18. y/ 2 + 44.y/2 =20,29 -18,74 → y = 0,05 mol
X tác dụng với 0,5 mol HCl :
M2CO3 + 2HCl → 2MCl + H2O + CO2
MHCO3 + HCl → MCl + H2O + CO2
nCO2 = x + y = 0,15 → x =0,1mol → nHCl phản ứng = 2.0,1 + 0,05 =0,25 mol < nHCl ban đầu
→ HCl dư
Dd Y có MCl và có thể có HCl dư
Ag+ + Cl- → AgCl
0,52 mol
→ nCl- = 0,52 = nHCl + nMCl (ban đầu) = 0,5 + z → z = 0,02 mol
Ta có mX = 0,1 (2M + 60) + 0,05 ( M + 61) + 0,02 (M + 35,5) → M = 39 (K)
Trong KCl thì %K = 39/74,5 .100% =52,35 %

Chọn C
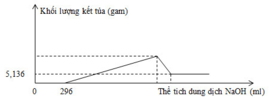
Vì: Quan sát đồ thị ta thấy:
mFe(OH)3 = 5,236 gam => nFe(OH)3 = 0,048 mol
nHNO3 dư = 0,296 mol => nHNO3 pư = 0,8 – 0,296 = 0,504 mol
Phần 1: Cho X tác dụng với H2SO4 đặc cũng như cho hỗn hợp đầu tác dụng
BT e: 3nAl = 2nSO2 => nAl = 2.0,09/3 = 0,06 mol
Phần 2: Cho X tác dụng với HNO3 cũng như cho hỗn hợp đầu tác dụng
Al + 4HNO3 → Al(NO3)3 + NO + 2H2O
0,06→0,24
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
0,024←0,144←0,048
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
0,02 ←0,504-0,24-0,144 = 0,12
mCr2O3 (1 phần) = 0,02.152 = 3,04 gam
=> mCr2O3 = 6,08 gam