cho 2.24l khí metan(đktc) phản ứng hoàn toàn với V lít khí Clo cùng điều kiện,thu được chất A và HCl. Biết Clo chiến 83,53% khối lượng A.Tìm V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, PT: \(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
Ta có: \(n_{MnO_2}=\dfrac{30,45}{87}=0,35\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Cl_2}=n_{MnO_2}=0,35\left(mol\right)\\n_{HCl}=4n_{MnO_2}=1,4\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Cl_2}=0,35.71=24,85\left(g\right)\)
\(V_{ddHCl}=\dfrac{1,4}{1}=1,4\left(l\right)\)
b, PT: \(2Fe+3Cl_2\underrightarrow{t^o}2FeCl_3\)
Ta có: \(n_{Fe}=\dfrac{25,2}{56}=0,45\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,45}{2}>\dfrac{0,35}{3}\), ta được Fe dư.
Theo PT: \(n_{FeCl_3}=\dfrac{2}{3}n_{Cl_2}=\dfrac{7}{30}\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=\dfrac{7}{30}.162,5\approx37,9\left(g\right)\)
Bạn tham khảo nhé!

Phương trình hóa học của phản ứng:
M + n/2HCl → M Cl n
M + mHCl → M Cl m + m/2 H 2
Theo đề bài, ta có:
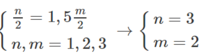
và M + 106,5 = 1,2886 (M+71)
Giải ra, ta có M = 52 (Cr)

Bài 1:
PTHH: \(CH_4+Cl_2\underrightarrow{a/s}CH_3Cl+HCl\)
Theo PTHH: \(n_{Cl_2}=n_{CH_3Cl}=n_{CH_4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}m_{CH_3Cl}=0,15\cdot50,5=7,575\left(g\right)\\V_{CH_4}=V_{Cl_2}=3,36\left(l\right)\end{matrix}\right.\)
Bài 2:
PTHH: \(CH_4+2O_2\underrightarrow{a/s}CO_2+2H_2O\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{CO_2}=n_{CH_4}\\n_{O_2}=2n_{CH_4}\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}V_{CO_2}=V_{CH_4}=5,6\left(l\right)\\V_{CO_2}=2V_{CH_4}=11,2\left(l\right)\end{matrix}\right.\)

b1: viết pthh
cl2+ h2-> 2hcl
b2: tính số mol cá chất dựa vào khối lượng hoăc thể tích đề bài cho
nH2= 67,2/224=3 mol
b3: dựa vào phương trình tính số mol các chất còn lại
theo pthh: ncl2=nh2=3 mol
nhcl=2nh2=3*2=6 mol
b4: tính khối lượng hoặc thể tích chất đề bài yêu cầu
=> Vcl2= 3*22,4=67,2l
mhcl=6* 36,5= 219g
CHÚC BẠN HỌC TỐT!

Có: nH2= 67,2:22,4=3(mol)
PTPƯ: H2 + Cl2 --to--> 2 HCl
(mol) 1 1 2
(mol) 3 3 6
(l) 67,2 67,2 134,4
(g) 6 213 219

Câu 1:
PTHH: \(Na+\dfrac{1}{2}Cl_2\xrightarrow[]{t^o}NaCl\)
Ta có: \(n_{NaCl}=2n_{Cl_2}=2\cdot\dfrac{2,24}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,2\cdot58,5=11,7\left(g\right)\)
Câu 2:
Ta có: \(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\) \(\Rightarrow m_{H_2}=0,04\cdot2=0,08\left(g\right)\)
Bảo toàn nguyên tố: \(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\) \(\Rightarrow m_{HCl}=0,08\cdot36,5=2,92\left(g\right)\)
Bảo toàn khối lượng: \(m_{muối}=m_{KL}+m_{HCl}-m_{H_2}=4,29\left(g\right)\)

Chúc em học tốt !!!
\(a.\)
\(n_{Na}=\dfrac{4.6}{23}=0.2\left(mol\right)\)
\(Na+\dfrac{1}{2}Cl_2\underrightarrow{t^0}NaCl\)
\(0.2........0.1........0.2\)
\(V_{Cl_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{NaCl}=0.2\cdot58.5=11.7\left(g\right)\)
\(b.\)
\(n_{Fe}=\dfrac{5.6}{56}=0.1\left(mol\right)\)
\(Fe+\dfrac{3}{2}Cl_2\underrightarrow{t^0}FeCl_3\)
\(0.1.......0.15.......0.1\)
\(V_{Cl_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(m_{FeCl_3}=0.1\cdot162.5=16.25\left(g\right)\)
\(c.\)
\(n_{Cu}=\dfrac{6.4}{64}=0.1\left(mol\right)\)
\(Cu+Cl_2\underrightarrow{t^0}CuCl_2\)
\(0.1......0.1.....0.1\)
\(V_{Cl_2}=0.1\cdot22.4=2.24\left(l\right)\)
\(m_{CuCl_2}=0.1\cdot135=13.5\left(g\right)\)
Bài 1:
a. \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
\(2Na+Cl_2\rightarrow2NaCl\)
0,2 ...... 0,1 ..... 0,2 (mol)
\(\rightarrow\left\{{}\begin{matrix}V_{Cl_2}=0,1.22,4=2,24\left(l\right)\\m_{NaCl}=0,2.58,5=11,7\left(g\right)\end{matrix}\right.\)
b. \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
0,1 ...... 0,15 ...... 0,1 (mol)
\(\rightarrow\left\{{}\begin{matrix}V_{Cl_2}=0,15.22,4=3,36\left(l\right)\\m_{FeCl_3}=0,1.162,5=16,25\left(g\right)\end{matrix}\right.\)
c. \(n_{Cu}=\dfrac{6,4}{64}=0,1\left(mol\right)\)
\(Cu+Cl_2\rightarrow CuCl_2\)
0,1 .... 0,1 ..... 0,1 (mol)
\(\rightarrow\left\{{}\begin{matrix}V_{Cl_2}=0,1.22,4=2,24\left(l\right)\\m_{CuCl_2}=0,1.135=13,5\left(g\right)\end{matrix}\right.\)

có: nCH4= \(\dfrac{2,24}{22,4}\)= 0,1( mol)
PTPU
CH4+ Cl2\(\xrightarrow[]{as}\) CH3Cl+ HCl
0,1......0,1..........0,1............. mol
\(\Rightarrow\) mCH3Cl= 0,1. 50,5= 5,05( g)
\(\Rightarrow\) mA= \(\dfrac{5,05}{100\%-83,53\%}\)= 30,66( g)
\(\Rightarrow\) mCl2= 30,66. 83,53%= 25,61( g)
\(\Rightarrow\) \(\sum nCl2\)= \(\dfrac{25,61}{71}\)+ 0,1= 0,46( mol)
\(\Rightarrow\) VCl2= 0,46. 22,4= 10,304( lít)