Để hòa tan hết hỗn hợp Zn và ZnO phải dùng 100,8ml dung dịch HCl 36,5%(d=1,19 g/ml) thu được 0,4 mol khí. Thành phần phần trắm về khối lượng của Zn và ZnO trong hỗn hợp ban đầu lần lượt là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
![]() .100 => mHCl = 43,78 (g)
.100 => mHCl = 43,78 (g)
nHCl = 1,2 (mol)
Gọi nZn = a, nZnO = b
Zn + 2HCl → ZnCl2 + H2
0,4 0,8 ← 0,4 (mol)
ZnO + 2HCl → ZnCl2 + H2O
0,2 ← 0,4 (mol)
![]() .100%
.100%
![]() .100% = 61,61%
.100% = 61,61%
%mZnO = 100% -61,6% = 38,4%

Giải thích:
Zn + 2HCl -> ZnCl2 + H2
ZnO + 2HCl -> ZnCl2 + H2O
nH2 = nZn = 0,4 mol
nHCl = 1,2 mol = 2nZn + 2nZnO => nZnO = 0,2 mol
=> %mZnO = 38,4%
Đáp án B

a)\(n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,15 0,3 0,15
\(m_{Zn}=0,15\cdot65=9,75\left(g\right)\)
\(\%m_{Zn}=\dfrac{9,75}{17,85}\cdot100\%=54,62\%\)
\(\%m_{ZnO}=100\%-54,62\%=45,38\%\)
b)\(m_{ZnO}=17,85-9,75=8,1\left(g\right)\Rightarrow n_{ZnO}=\dfrac{8,1}{81}=0,1mol\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
0,1 0,2
\(\Rightarrow\Sigma n_{HCl}=0,3+0,2=0,5mol\)
\(\Rightarrow V=\dfrac{0,5}{1}=0,5l=500ml\)

\(n_{HCl} = \dfrac{448.1,12.3,65\%}{36,5} = 0,50176(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ ZnO + 2HCl \to ZnCl_2 + H_2O\\ n_{Zn} = n_{H_2} = \dfrac{2,24}{22,4} = 0,1(mol)\\ n_{ZnO} = \dfrac{n_{HCl} - 2n_{Zn}}{2} = \dfrac{0,50176-0,1.2}{2} = 0,15088(mol)\\ \%m_{Zn} = \dfrac{0,1.65}{0,1.65 + 0,15088.81}.100\% = 34,72\%\\ \%m_{ZnO} = 65,28\%\)

Tiếp bài của creeper nhé:
c. Ta có: \(n_{ZnO}=\dfrac{4,86}{81}=0,06\left(mol\right)\)
Theo PT(1): \(n_{HCl}=2.n_{ZnO}=2.0,06=0,12\left(mol\right)\)
Theo PT(2): \(n_{HCl}=2.n_{Zn}=2.0,1=0,2\left(mol\right)\)
=> \(n_{HCl}=0,12+0,2=0,32\left(mol\right)\)
=> \(m_{HCl}=0,32.36,5=11,68\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{11,68}{m_{dd_{HCl}}}.100\%=12\%\)
=> \(m_{dd_{HCl}}=\dfrac{292}{3}\left(g\right)\)
Theo đề, ta có:
\(D=\dfrac{\dfrac{292}{3}}{V_{dd_{HCl}}}=1,2\)(g/ml)
=> \(V_{dd_{HCl}}=81,1\left(ml\right)\)

Zn +2 HCl ---> ZnCl2 + H2
0,1-----0,2----------0,1-------------0,1 mol
ZnO + 2HCl ---> ZnCl2 + H2O
0,2------0,4-------0,2--------0,2
n H2=\(\dfrac{2,24}{22,4}=0,1mol\)
=>m Zn=0,1.65=6,5g
=>m HCl(1)=0,2.36,5=7,3g
=>m HCl(2)=14,6g -> nHCl=0,4 mol
=>%m Zn=\(\dfrac{6,5}{6,5+14,4}.100=31,1\%\)
=>%m ZnO=68,9%
b)
->m HCl=0,6.36,5=21,9g
->m ZnCl2=0,3.136=40,8g

\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
Ta có:
\(n_{H2}=n_{Zn}=\frac{8,96}{22,4}=0,4\left(mol\right)\Rightarrow m_{Zn}=0,4.65=26\left(g\right)\)
m dung dịch HCl=100,9.1,19=120 gam
-> m HCl=120.36,5%=43,8 gam
-> nHCl=43,8/36,5=1,2 mol
nHCl=2nZn + 2nZnO
-> nZnO=0,2 mol -> mZnO=0,2.(65+16)=16,2 gam
nZnCl2=nZnO + nZn=0,6 mol
-> mZnCl2=0,6.(65+35,5.2)=81,6 gam
BTKL: m rắn + m dung dịch HCl= m dung dịch sau phản ứng + mH2
-> m dung dịch sau phản ứng = 26+16,2+120-0,4.2=161,4 gam
-> C% ZnCl2=81,6/161,4=50,55%

\(n_{H_2}=\dfrac{4.48}{22.4}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2.........0.4.........0.2......0.2\)
\(m_{Zn}=0.2\cdot65=13\left(g\right)\Rightarrow m_{ZnO}=14.6-13=1.6\left(g\right)\)
\(\%Zn=\dfrac{13}{14.6}\cdot100\%=89.04\%\)
\(\%ZnO=100\%-89.04\%=10.96\%\)
\(n_{ZnO}=\dfrac{1.6}{81}\approx0.02\left(mol\right)\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
\(0.02........0.04........0.02........0.02\)
\(n_{HCl}=0.4+0.04=0.44\left(mol\right)\)
\(C_{M_{HCl}}=\dfrac{0.44}{0.8}=0.55\left(M\right)\)
Eeeee ngồi tính sang chấn thật nó ra số xấu lần mò hơn 20p chưa biết tính sai chỗ nào
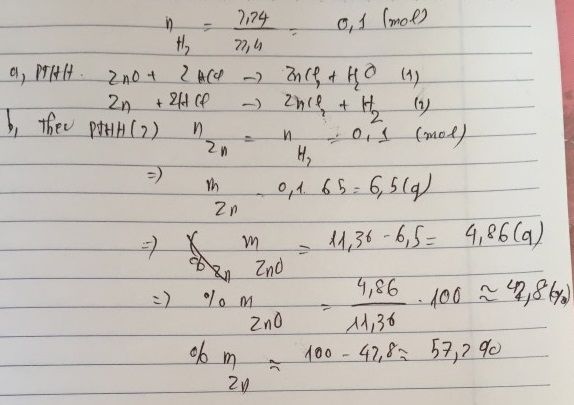
mdd HCl = 100,8.1,19 = 119,952 (g)
=> mHCl = \(\dfrac{119,952.36,5\%}{100\%}\)= 43,8 (g)
=> nHCl = \(\dfrac{43,8}{36,5}\)= 1,2 (mol)
Zn + 2HCl ----> ZnCl2 + H2
0,4 0,8 0,4 0,4 (mol)
=> mZn = 0,4.65 = 26 (g)
ZnO + HCl ----> ZnCl2 + H2O
0,4 0,4 0,4 0,4 (mol)
=> mZnO = 0,4.81 = 32,4 (g)
=> mhỗn hợp ban đầu = 26 + 32,4 = 58,4 (g)
=> %Zn = \(\dfrac{26.100\%}{58,4}\)= 44,52%
=> %ZnO = \(\dfrac{32,4.100\%}{58,4}\)= 55,48%
dạ hình như pt ZnO chưa cân bằng ạ!