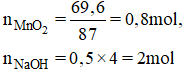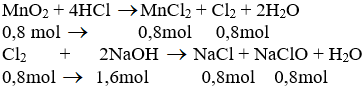Cho 2,61 gam MnO2 vào 18,25 gam dung dịch HCl 30% sau phản ứng thu được dung dịch a và khí b dẫn khí thu được sau phản ứng dẫn qua 50 ml dung dịch NaOH 2 m ở nhiệt độ thường thu được dung dịch X
a)Tính nồng độ phần trăm chất trong dung dịch a b)Tính nồng độ mol lít chất trong dung dịch X Giả sử thể tích dung dịch không thay đổiHãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Số mol các chất là:
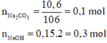
Na2CO3 tác dụng với dung dịch HCl dư:
Sơ đồ phản ứng:
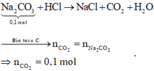
Xét giai đoạn hấp thụ CO2 vào dung dịch NaOH:
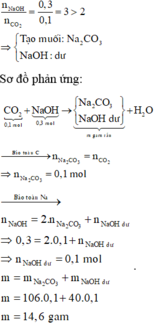

Đáp án C
![]() = 0,8 mol
= 0,8 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 → ![]() = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M

Đáp án C
nCaCO3 = 20: 100 = 0,2 mol
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Mol: 0,2 → 0,2
nNaOH = 0,1.2,5 = 0,25 mol
Ta thấy: nCO2 < nNaOH < 2nCO2 => phản ứng tạo hỗn hợp muối NaHCO3 và Na2CO3

a) Phương trình hóa học của phản ứng:
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 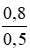
CM (NaOH)dư = 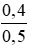
tích cho mình nha![]()

\(a,n_{Na_2SO_3}=\dfrac{12,6}{126}=0,1mol\\ Na_2SO_3+2HCl\rightarrow2NaCl+SO_2+H_2O\\ n_{SO_2}=n_{Na_2SO_4}=0,1mol\\ V_{SO_2}=0,1.22,4=2,24l\\ b,n_{HCl}=0,1.2=0,2mol\\ C_{M_{HCl}}=\dfrac{0,2}{0,15}=\dfrac{4}{3}M\\ c,n_{NaOH}=\dfrac{40.10}{100.40}=0,1mol\\ T=\dfrac{0,1}{0,1}=1\\ \Rightarrow Tạo,NaHSO_3\\ NaOH+SO_2\rightarrow NaHSO_3\\ m_{NaHSO_3}=0,1.64+0,1.40=10,4g\)

\(n_{KMnO_4} = \dfrac{15,8}{158} = 0,1(mol)\\ n_{HCl} = 0,08.2 = 0,16(mol)\)
2KMnO4 + 16HCl \(\to\) 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,02.............0,16...................................0,05..............(mol)
\(n_{NaOH} = 0,2.1,5 = 0,3(mol)\)
2NaOH + Cl2 \(\to\) NaCl + NaClO + H2O
0,1..........0,05......0,05......0,05........................(mol)
Vậy :
\(C_{M_{NaCl}} = C_{M_{NaClO}} = \dfrac{0,05}{0,2}= 0,25M\\ C_{M_{NaOH}} = \dfrac{0,3-0,1}{0,2} = 1M\)