nhiệt phân 4,385 g hh X gồm KClO3 và KMnO4 thu được O2 và m gam chất rắn gồm K2MnO4 MnO2 và KCl. Toàn bộ lượng O2 tác dung hết với cacbon nóng đỏ, thu được 0,896 lít hỗn hợp khí Y( đktc) có tỉ khối so với H2 là 16. Tính thành phần % theo khối lượng của KMnO4 trong X
GIÚP EM VỚI EM CẦN GẤP Ạ!!! @Cẩm Vân Nguyễn Thị @Trần Hữu Tuyển @Phùng Hà Châu

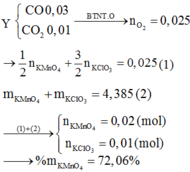
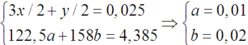
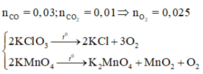
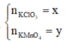
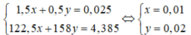
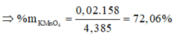


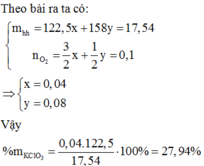
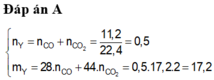
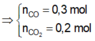
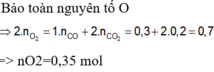
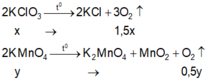
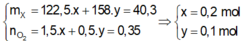



PTHH : 2KClO3 --to--> 2KCl + 3O2 (1)
2KMnO4--to--> K2MnO4 + MnO2 + O2 (2)
C + O2 --to--> CO2 (3)
2C + O2 --to--> 2CO (4)
Theo đề ra : \(n_Y=\dfrac{V}{22,4}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)(I)
Mà \(d_{\dfrac{Y}{H_2}}=16\Rightarrow M_Y=16\cdot2=32\)
ta có sơ đồ đường chéo :
\(\Rightarrow\dfrac{n_{CO2}}{n_{CO}}=\dfrac{32-28}{44-32}=\dfrac{1}{3}\)(II)
Từ I và II =>
\(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}=0,01\left(mol\right)\\n_{CO}=0,03\left(mol\right)\end{matrix}\right.\)
theo PT 3,4
=> nO2 = \(0,01+\dfrac{0,03}{2}=0,025\left(mol\right)\)
gọi a,b lần lượt là số mol của KClO3 và KMnO4
THEO : PT1 : n\(n_{O_2}=\dfrac{3}{2}a\)
PT2 : \(n_{O_2}=0,5a\)
ta có hệ PT
\(\left\{{}\begin{matrix}122,5a+158b=4,385\\\dfrac{3}{2}a+0,5b=0,025\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\)
\(m_{KMnO_4}=0,02\cdot158=3,16\left(g\right)\)
\(\%KMnO_4=\dfrac{3,16}{4,385}\cdot100\%\approx72,06\%\)
HOK TỐT
nY = 0.04 mol, vì My = 16*2 = 32 nên Y gồm CO & CO2.
Gọi a = nCO, b = nCO2 = > a + b = 0.04. Từ My = 32
= > (28a + 44b)/(a + b) = 32 <= > 4a – 12b = 0 <= > a – 3b = 0
= > a = 0.03, b = 0.01.
= > nO2 = nCO/2 + nCO2 = 0.03/2 + 0.01 = 0.025 (ĐCGĐ).
KMnO4 (x mol) >>>>>>>>> 1/2xO2
KClO2 (y mol) >>>>>>>>> 3/2yO2
= > 158x + 106.5y = 4.385 & x/2 + 3x/2 = 0.025
= >x = 0.02, y = 0.01
= > %mKMnO4 = 0.02*158/4.385 = 72.06%