Bài 4. Cho 120 gam dung dịch MgCl2 19% vào dung dịch Ba(OH)2 dư. Lấy kết tủa thu được đem nung đến khối lượng không đổi được bao nhiêu gam chất rắn?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


ĐÁP ÁN B:
Do sắt dư nên phản ứng HNO3 chỉ tạo muối sắt 2
3Fe + 8H+ + 2NO3- ->3Fe2+ + 2NO + 4H2O
Mol 0,3 <- 0,8
Sơ đồ : Fe => Fe2+ => Fe(OH)2 => Fe2O3
Theo DLBT nguyrn tố Fe ta có => n Fe2O3 = ½ nFe = 0,15 mol => m rắn = m Fe2O3 = 24g
=> chọn B

Đáp án : B
VÌ có sắt dư nên chỉ tạo Fe2+
3Fe + 8H+ + 2NO3- -> 3Fe2+ + 2NO + 4H2O
=> nFe = 3/8nH+ = 0,3 mol = nFe2+
=> nFe2+ = nFe(OH)2 = 2nFe2O3
=> nFe2O3 = 0,15 mol => mrắn =24g

Đáp án C
Qui hỗn hợp A thành
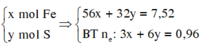
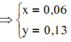
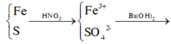

=> mrắn = mFe2O3 + mBaSO4 = 0,03.160 + 0,13.233 = 35,09g

n MgCl2 = a(mol) ; n ZnSO4 = b(mol)
=> 95a + 161b = 67,3(1)
MgCl2 + 2KOH → Mg(OH)2 + 2KCl
ZnSO4 + 2KOH → Zn(OH)2 + 2KCl
Zn(OH)2 + 2KOH → K2ZnO2 + 2H2O
$Mg(OH)_2 \xrightarrow{t^o} MgO + H_2O$
=> 40a = 8(2)
Từ (1)(2) suy ra a = 0,2 ; b = 0,3
=>m ZnSO4 = 0,3.161 = 48,3 gam

\(a)n_K=\dfrac{7,8}{39}=0,2mol\\ 2K+2H_2O\rightarrow2KOH+H_2\\ n_{H_2}=2n_K=0,4mol\\ V_{H_2\left(đktc\right)}=0,4.22,4=8,96l\\ V_{H_2\left(đkc\right)}=0,4.24,79=9,916g\\ b)n_{KOH}=n_K=0,2mol\\ 2KOH+Cu\left(NO_3\right)_2\rightarrow2KNO_3+Cu\left(OH\right)_2\\ n_{Cu\left(OH\right)_2}=\dfrac{1}{2}n_{KOH}=0,1mol\\ m_{\downarrow}=m_{Cu\left(OH\right)_2}=0,1.98=9,8g\\ c)Cu\left(OH\right)_2\xrightarrow[]{t^0}CuO+H_2O\\ n_{CuO}=n_{Cu\left(OH\right)_2}=0,1mol\\ m_{CuO}=0,1.80=8g\)

Tính toán theo PTHH :
Mg + CuSO4 → Cu + MgSO4
Mg + FeSO4 → Fe + MgSO4
Ba(OH)2 + MgSO4 → BaSO4 + Mg(OH)2
Ba(OH)2 + FeSO4 → BaSO4 + Fe(OH)2
Mg(OH)2 → MgO + H2O
2 Fe(OH)2 + ½ O2 → Fe2O3 + 2 H2O
Giả sư dung dịch muối phản ứng hết
=> n Fe = n FeSO4 = 0,2 . 1= 0,2 mol => m Fe = 0,2 . 56 = 11,2 g
=> n Cu =n CuSO4 = 0,2 . 0,5 = 0,1 mol => m Cu = 0,1 . 64 = 6,4 g
=> m chất rắn = 11,2 + 6,4 = 17,6 g > 12 g > 6,4
=> kim loại Fe dư sau phản ứng Vì CuSO4 phản ứng trước sau đó mới đến FeSO4 phản ứng
CuSO4 đã hết và phản ứng với 1 phần FeSO4
12 g = m Cu + m Fe phản ứng = 6,4 g + m Fe phản ứng
=> m Fe = 5,6 g => n Fe = 0,1 mol => n FeSO4 dư = 0,2 – 0,1 = 0,1 mol
Theo PTHH : n Mg = 0,1 + 0,1 = 0,2 mol ( bắng số mol CuSO4 và FeSO4 phản ứng )
Theo PTHH : n Mg = n MgSO4 = n Mg(OH)2 = n MgO = 0,2 mol
n FeSO4 dư = n Fe(OH)2 = n Fe2O3 . 2 = 0,1 mol
=> n Fe2O3 = 0,1 mol
=> m chất rắn = m Fe2O3 + m MgO = 0,1 . 160 + 0,2 . 40 = 24 g

Gọi x, y, z lần lượt là số mol Al3+ , Fe2+, SO42- trong dung dịch X. Ta có: nCl- = 3x + 2y - 2z (bảo toàn điện tích)
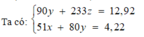
m = 162,5x + 127y + 25z
⇒ 7,58 <m< 14,83
Đáp án D
Bài 4 :
\(m_{ct}=\dfrac{19.120}{100}=22,8\left(g\right)\)
\(n_{MgCl2}=\dfrac{22,8}{95}=0,24\left(mol\right)\)
Pt : \(MgCl_2+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2+BaCl_2|\)
1 1 1 1
0,24 0,24
Pt : \(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O|\)
1 1 1
0,24 0,24
\(n_{MgO}=\dfrac{0,24.1}{1}=0,24\left(mol\right)\)
⇒ \(m_{MgO}=0,24.40=9,6\left(g\right)\)
Chúc bạn học tốt