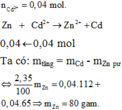Bài 2: Ngâm một lá nhôm có khối lượng 10 gam vào 500 ml dung dịch đồng (II) sunfat 0,4M cho tới khi nhôm không thể tan thêm được nữa. Lấy lá nhôm ra, rửa nhẹ, làm khô và cân thì thấy khối lượng là 11,38 g. a. Tính khối lượng đồng thoát ra bám vào miếng nhôm? b. Tính nồng độ mol của các chất thu được sau phản ứng.Biết thể tích dung dịch thay đổi ko đáng kể.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
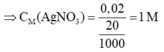
⇒ Chọn C.

\(m_{ZnSO_4}=\dfrac{241,5.10}{100}=24,15\left(g\right)=>n_{ZnSO_4}=\dfrac{24,15}{161}=0,15\left(mol\right)\)
PTHH: 2Al + 3ZnSO4 --> Al2(SO4)3 + 3Zn
_____0,1<----0,15-------->0,05----->0,15
=> mAl = 0,1.27 = 2,7(g)
=> mZn = 0,15.65=9,75(g)
b) mdd sau pư = 2,7 + 241,5 - 9,75 = 234,45(g)
=> \(C\%\left(Al_2\left(SO_4\right)_3\right)=\dfrac{0,05.342}{234,45}.100\%=7,294\%\)

a)
Gọi số mol CuCl2 phản ứng là a (mol)
PTHH: 2Al + 3CuCl2 --> 2AlCl3 + 3Cu
____\(\dfrac{2}{3}a\)<-----a--------------------->a
=> \(20-\dfrac{2}{3}a.27+64a=33,8\)
=> a = 0,3 (mol)
=> mCu = 0,3.64 = 19,2(g)
b)
\(C_{M\left(ddCuCl_2\right)}=\dfrac{0,3}{0,15}=2M\)