Cho ống thủy tinh chứa 48,8 g hỗn hợp X gồm FeO và Fe2O3 đã được đốt nóng. Cho dòng khí H2 đi chậm qua X đến dư. Phản ứng xong, trong ống còn lại 39,2 g Fe.Mặt khác, nếu cho 24,4 g hỗn hợp X vào dung dịch CuSO4 dư, lắc kỹ và để phản ứng hoàn toàn, lọc lấy chất rắn, làm khô, cân nặng m gam. Tính khối lượng từng chất trong 48,8 g hỗn hợp X và tính m (gam)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

phương trình phản ứng
FeO + H2 = Fe + H2O (1)
y y mol
Fe2O3 + 3H2 = 2Fe + 3H2O (2)
z 2z mol
Fe + CuSO4(dung dịch pha loãng) = FeSO4 + Cu↓ (3)
x x mol
theo phương trình phản ứng (3) áp dụng định luật thay đổi khối lhuowngj ta có 64x - 56x = 4,96 - 4,72 => x=0,03 mol
khối lượng của Fe là mFe = 0,03.56=1,68(g)
khối lượng của oxit sắt còn lại là 3,04 g
theo bài ra ta có phương trình
72y + 160z = 3,04
56y + 56.2z = 3,92 - 1,68
giải hệ phương trình ta có y= 0,02 z= 0,01
còn lại khối lượng bạn tự tính nha![]()

\(FeO+H_2\underrightarrow{t^o}Fe+H_2O\)
y y
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
z 2z
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
x x
gọi x, y, z là số mol của Fe bđ, FeO bđ, \(Fe_2O_3bđ\)
có: \(\left\{{}\begin{matrix}56x+56y+\left(56.2\right)z=2,94\\56x+72y+160z=3,54\\64x+72y+160z=3,72\end{matrix}\right.\)
Giải được:
x = 0,0225
y = 0,015
z = 0,0075
=> m Fe bđ = 0,0225 . 56 = 1,26 (g)
m FeO bđ = 0,015.72 = 1,08 (g)
m \(Fe_2O_3\) bđ = 0,0075 . 160 = 1,2 (g)
( Với hệ pt:
- ở dòng 1, 56x, 56y, 112z là của pt Fe không td vs H2, pt FeO bị H2 khử và pt \(Fe_2O_3\) bị \(H_2\) khử.
- ở dòng 2, 56x: m Fe bđ
72y: m FeO bđ
160z: m \(Fe_2O_3\) bđ
- ở dòng 3, 64x: \(m_{Cu}\) khi Fe td với \(dd.CuSO_4\) tạo được x mol Cu
72y: m FeO không td với dd CuSO4
160z: m \(Fe_2O_3\) không td với dd \(CuSO_4\) )

Khí CO khử được oxit của các kim loại đứng sau Al thành kim loại tương ứng và khí C O 2 .
C O + C u O - t 0 → C u + C O 2
3 C O + F e 2 O 3 - t 0 → 2 F e + 3 C O 2
⇒ Chọn B.

Giải thích: Đáp án A
n BaCO3 = n CO2 = 9,062 : 197 = 0,046 mol
=> n O đã pư = 0,046 mol => m O = 0,736 g
Bảo toàn khối lượng m hhđầu = m O pư + m hh sau = 0,736 + 4,784 = 5,52 g
Ta có hệ 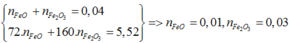
=> m FeO = 0,72 g
=> % m FeO = 13,04%
Chú ý : Bản chất của phản ứng dùng CO hay H2 khử oxit kim loại là việc CO hay H2 lấy O trong oxit ra tạo thành CO2 và H2O , số mol CO , H2 sẽ bằng số mol O ( nằm trong oxit ) đã bị lấy ra

Đáp án D
nCO2 = nBACO3 = 9,062/197 = 0,046
BTKL => mX = mY + mCO2 – mCO = 4,784 + 0,046(44 – 28) = 5,52
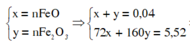
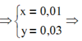
%mFeO = 0,01.72.100%/5,52 = 13,04%

Đáp án D
nCO2 = nBACO3 = 9,062/197 = 0,046
BTKL => mX = mY + mCO2 – mCO = 4,784 + 0,046(44 – 28) = 5,52
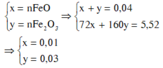
=> %mFeO = 0,01.72.100%/5,52 = 13,04%