CACO3->CAC+CO2
chất tham gia phản ứng là chất nàoHãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


1) \(m_{CO_2}=m_{rắn\left(trcpư\right)}-m_{rắn\left(saupư\right)}=100-64,8=35,2\left(g\right)\)
=> \(n_{CO_2}=\dfrac{35,2}{44}=0,8\left(mol\right)\)
=> \(V_{CO_2}=0,8.22,4=17,92\left(l\right)\)
2)
PTHH: CaCO3 --to--> CaO + CO2
0,8<---------0,8<---0,8
=> \(m_{CaCO_3\left(pư\right)}=0,8.100=80\left(g\right)\)
3)
\(m_{CaCO_3\left(bd\right)}=\dfrac{100.90}{100}=90\left(g\right)\)
=> Rắn sau pư chứa CaCO3, CaO, tạp chất
\(m_{tạp.chất}=100-90=10\left(g\right)\)
\(m_{CaCO_3\left(saupư\right)}=90-80=10\left(g\right)\)
\(m_{CaO}=0,8.56=44,8\left(g\right)\)
\(1,n_{CaCO_3}=\dfrac{90\%.100}{100}=0,9\left(mol\right)\\ PTHH:CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ Đặt:n_{CaCO_3\left(p.ứ\right)}=a\left(mol\right)\left(a>0\right)\\ Ta.có:m_{rắn}=64,8\left(g\right)\\ \Leftrightarrow10+\left(90-100a\right)+56a=64,8\\ \Leftrightarrow a=0,8\left(mol\right)\\ n_{CO_2}=n_{CaO}=n_{CaCO_3\left(p.ứ\right)}=0,8\left(mol\right)\\ V_{CO_2\left(đktc\right)}=0,8.22,4=17,92\left(l\right)\\ 2,m_{CaCO_3\left(p.ứ\right)}=0,8.100=80\left(g\right)\\ 3,Rắn.sau.nung:m_{tạp.chất}=10\%.100=10\left(g\right)\\ m_{CaO}=0,8.56=44,8\left(g\right)\\ m_{CaCO_3\left(dư\right)}=\left(0,9-0,8\right).100=10\left(g\right)\)

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 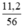 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 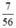 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 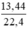 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

1. Na + 1/2O2 -> NaO
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
AgNO3 + NaCl -> AgCl + NaNO3
CuSO4 + 2NaOH -> Na2SO4 + Cu(OH)2

Phương trình hóa học CaCO\(_3\) → CaO + CO\(_2\).
a) nCaO = \(\frac{11,2}{56}\) = 0,2 mol.
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,2 (mol)
b) nCaO = \(\frac{7}{56}\) = 0,125 (mol)
Theo PTHH thì nCaCO\(_3\) = nCaO = 0,125 (mol)
mCaCO\(_3\) = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO\(_2\) = nCaCO\(_3\) = 3,5 (mol)
VCO\(_2\) = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO\(_2\) = \(\frac{13,44}{22,4}\) = 0,6 (mol)
Theo PTHH nCaO = nCaCO\(_3\) = nCO\(_2\) = 0,6 (mol)
mCaCO\(_3\) = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)
#shin

\(a.2Al+3CuCl_2\rightarrow2AlCl_3+3Cu\)
Tỉ lệ = \(2:3:2:3\)
\(b.2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
Tỉ lệ = \(2:1:1:2\)
\(c.CaO+2HCl\rightarrow CaCl_2+H_2O\)
Tỉ lệ = \(1:2:1:1\)
\(d.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Tỉ lệ = \(1:1:1:1\)
a.2Al+3CuCl2→2AlCl3+3Cua.2Al+3CuCl2→2AlCl3+3Cu
b.2NaOH+H2SO4→Na2SO4+2H2Ob.2NaOH+H2SO4→Na2SO4+2H2O
c.CaO+2HCl→CaCl2+H2Oc.CaO+2HCl→CaCl2+H2O
d.Ca(OH)2+CO2→CaCO3+H2Od.Ca(OH)2+CO2→CaCO3+H2O

Chất tham gia phản ứng là: CaCO3
Chất tham gia phản ứng là CaCO3 có to bạn nhé