Cho 5,4g Al vào dung dịch H2SO4 2M thu được dung dịch B và thể tích H2 (dktc) A.tính thể tích H2(dktc) B.tính thể tích H2SO4 2M C.tính khối lượng muối Giúp mình với.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)=n_{H_2SO_4}=n_{ZnSO_4}\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{H_2SO_4}}=\dfrac{0,2}{0,2}=1\left(M\right)\\m_{ZnSO_4}=0,2\cdot161=32,2\left(g\right)\end{matrix}\right.\)
*Bạn bổ sung thêm khối lượng riêng của axit để tính C% nhé !

a, \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\Rightarrow V_{H_2}=0,3.24,79=7,437\left(l\right)\)
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
b, \(n_{H_2SO_4}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{0,3}{2}=0,15\left(l\right)\)

\(n_{Zn}=\dfrac{m}{M}=\dfrac{6,5}{65}=0,1\left(mol\right)\\ PTHH:Zn+H_2SO_4->ZnSO_4+H_2\)
tỉ lệ 1 ; 1 ; 1 ; 1
n(mol) 0,1-->0,1--------->0,1--------->0,1
\(V_{H_2\left(dktc\right)}=n\cdot22,4=0,1\cdot22,4=2,24\left(l\right)\\ m_{H_2SO_4}=n\cdot M=0,1\cdot\left(2+32+16\cdot4\right)=9,8\left(g\right)\\ m_{ZnSO_4}=n\cdot M=0,1\cdot\left(65+32+16\cdot4\right)=16,1\left(g\right)\)
a, \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
____0,1____0,1________0,1____0,1 (mol)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
b, \(m_{H_2SO_4}=0,1.98=9,8\left(g\right)\)
\(m_{ZnSO_4}=0,1.161=16,1\left(g\right)\)

a) \(n_{Mg}=\dfrac{12}{24}=0,5\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
0,5--->1------>0,5---->0,5
=> VH2 = 0,5.22,4 = 11,2 (l)
mHCl = 1.36,5 = 36,5 (g)
b) mMgCl2 = 0,5.95 = 47,5 (g)

\(\begin{array} {l} n_{Al}=\dfrac{5,4}{27}=0,2(mol)\\ n_{H_2SO_4}=\dfrac{39,2}{98}=0,4(mol)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ \dfrac{n_{Al}}{2}<\dfrac{n_{H_2SO_4}}{3}\to H_2SO_4\text{ dư}\\ n_{H_2}=\dfrac{3}{2}n_{Al}=0,3(mol)\\ V_{H_2(đktc)}=0,3.22,4=6,72(l) \end{array}\)

Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà n N O 2 = 3 n H 2 n ê n n e n h ư ờ n g ( 1 ) = n N O 2 n e n h ư ờ n g ( 2 ) = 2 n H 2
Nên ne nhường(1) =3/2 ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
n e n h ư ờ n g ( 1 ) n e n h ư ờ n g ( 2 ) = n R . h o a t r i 1 n p . h o a t r i 2 = 3 2
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
m R S O 4 = 62 , 81 % m R ( N O 3 ) 2
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là: n NO2= 3nFe=9
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
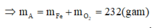
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:
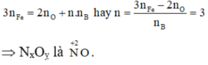
Khi đó:
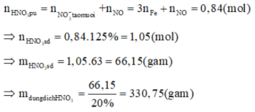

Đáp án C
Áp dụng định luật bảo toàn mol electron, ta có:
Mà nên
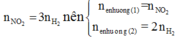
Nên ne nhường(1) = ne nhường(2)
Do đó số mol electron trao đổi ở hai trường hợp là không giống nhau nên R là kim loại có nhiều hóa trị.
Mà kim loại có hóa trị I, II hoặc III.
Kết hợp với
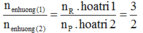
Ta được R có hóa trị II và III (trong đó R thể hiện hóa trị II khi tác dụng với dung dịch H2SO4 loãng và thể hiện hóa trị III khi tác dụng với dung dịch HNO3 đặc nóng).
Chọn 3 mol R đem hòa tan ban đầu. Khi đó ở các lần thí nghiệm ta thu được 3 mol R(NO3)3 và 3 mol RSO4.
Theo giả thiết ta có:
![]()
hay R + 96 = 62,81%(R +186)ÛR = 56ÞR là Fe.
Khi đó, áp dụng định luật bảo toàn moi electron ta có số mol NO2 tạo thành là:
![]()
Khi đó lượng oxi đã sử dụng là 9.22,22% = 2
![]()
A sẽ chứa một hoặc một số oxit của Fe. Để đơn giản cho quá trình tính toán, coi A là hỗn hợp chứa 3 mol Fe và 4 mol O.
Khi đó trong 20,88 gam A (20,88 = 0,09.232) có 0,27 mol Fe và 0,36 mol O.
nB = 0,03.
Gọi n là số mol electron mà x mol nguyên tử N + 5 nhận để thu được 1 mol NxOy
Áp dụng định luật bảo toàn mol electron, ta có:

Þ NxOỵ là .
Khi đó
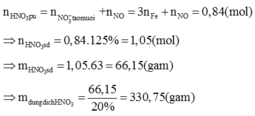
nAl = \(\dfrac{5,4}{27}=0,2\left(mol\right)\)
a. PTHH: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2.
Theo PT: \(n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\)
=> \(V_{H_2}=0,3.22,4=6,72\left(lít\right)\)
b. Theo PT: \(n_{H_2SO_4}=n_{H_2}=0,3\left(mol\right)\)
- Nếu là tính \(V_{dd_{H_2SO_4}}\) thì:
Ta có: \(C_{M_{H_2SO_4}}=\dfrac{0,3}{V_{dd_{H_2SO_4}}}=2M\)
=> \(V_{dd_{H_2SO_4}}=0,15\left(lít\right)\)
- Nếu tính \(V_{\left(đkxđ\right)}\) thì:
VÌ H2SO4 là chất lỏng nên thể tích bằng số mol của chính nó.
=> \(V_{H_2SO_4}=0,3\left(lít\right)\)
Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)
a,\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Mol: 0,2 0,3 0,1 0,3
\(V_{H_2}=0,3.22,4=3,36\left(l\right)\)
b, \(V_{ddH_2SO_4}=\dfrac{0,3}{0,2}=1,5M\)
c, \(m_{Al_2\left(SO_4\right)_3}=0,1.342=34,2\left(g\right)\)