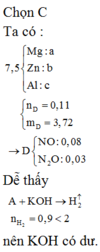Cho m g Mg vào trong 0.1 mol dung dịch HCl đến phản ứng kết thúc thì thấy cốc tăng lên 4.7 g .tính khối lượng MgCl2 thu đươc.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2} = \dfrac{15,6-14}{2} = 0,8(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Mg + 2HCl \to MgCl_2 + H_2\)
Gọi \(n_{Al} = a \ mol;n_{Mg} = b\ mol\)
Ta có :
\(\left\{{}\begin{matrix}27a+24b=15,6\\1,5a+b=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,4\\b=0,2\end{matrix}\right.\)
Vậy :
\(\%m_{Al} = \dfrac{0,4.27}{15,6}.100\% = 69,23\%\\ \%m_{Mg} = 100\% - 69,23\% = 30,77\%\)

Đáp án C
Fe3O4 + 8HCl -> FeCl2 + 2FeCl3 + 4H2O
1,4x -> 1,4x -> 2,8x
Cu + 2FeCl3 -> CuCl2 + 2FeCl2
x -> 2x
Y gồm : 0,06 mol MgCl2 ; x mol CuCl2 ; 3,4x mol FeCl2 ; 0,8x mol FeCl3
Điện phân đến khi anot xuất hiện khí :
Catot : 0,06 mol Mg2+ ; x mol Cu2+ ; 3,4x mol Fe2+ ; 0,8x mol Fe3+
Anot : (0,12 + 11,2x) mol Cl-
(Mg2+ không bị điện phân)
Vậy Catot : 2H2O + 2e -> H2 + 2OH-
Mol 0,12-> 0,06
mgiảm = mCu + mFe+ mH2 + mCl2
mmuối = mgiảm – mH2 + mMg (Vì bảo toàn e, số mol e H2 nhận đúng bằng số mol điện tích Mg2+ )
=> mmuối khan Y = 77,54 - 0,06.2 + 0,06.24 = 78,86g

Chọn C
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
1,4x → 1,4x → 2,8x
Cu + 2FeCl3 → CuCl2 + 2FeCl2
x → 2x
Y gồm : 0,06 mol MgCl2 ; x mol CuCl2 ; 3,4x mol FeCl2 ; 0,8x mol FeCl3
Điện phân đến khi anot xuất hiện khí :
Catot : 0,06 mol Mg2+ ; x mol Cu2+ ; 3,4x mol Fe2+ ; 0,8x mol Fe3+
Anot : (0,12 + 11,2x) mol Cl-
(Mg2+ không bị điện phân)
Vậy Catot : 2H2O + 2e → H2 + 2OH-
Mol 0,12→ 0,06
mgiảm = mCu + mFe+ mH2 + mCl2
mmuối = mgiảm – mH2 + mMg (Vì bảo toàn e, số mol e H2 nhận đúng bằng số mol điện tích Mg2+ )
=> mmuối khan Y = 77,54 - 0,06.2 + 0,06.24 = 78,86g