Câu 3 Khi cho một hỗn hợp gồm Na và K tác dụng hết với nước người ta thu được 3,36 lit khí hidro ( đktc ) và dung dịch A. Đem trung hoà dung dịch A bằng dung dịch HCl 25 % ( d = 1,05g / ml ) vừa đủ . Sau đó cô cạn thì thu được 19,5g hỗn hợp muối khan . a ) Tính thành phần phần trăm về khối lượng mỗi kim loại trong hỗn hợp . b ) Tính thể tích dung dịch axit HCl cần dùng .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$2Na + 2H_2O \to 2NaOH + H_2$
$Ba + 2H_2O \to Ba(OH)_2 + H_2$
$n_{H_2} = 0,15(mol)$
Theo PTHH :
$n_{OH^-} = 2n_{H_2} = 0,15.2 = 0,3(mol)$
Coi $V_{hh} = V(lít)$
Suy ra : $n_{HCl} = 0,5V; n_{HNO_3} = V$
Suy ra: $n_{H^+} = 0,5V + V = 1,5V(mol)$
$H^+ + OH^- \to H_2O$
Suy ra: $1,5V = 0,3 \Rightarrow V = 0,2(lít) = 200(ml)$

\(4.\)
\(n_{H_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.15.....0.3....................0.15\)
\(m_{Fe}=0.15\cdot56=8.4\left(g\right)\)
\(C_{M_{HCl}}=\dfrac{0.3}{0.5}=0.6\left(M\right)\)
\(5.\)
\(Đặt:n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=8.3\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{5.6}{22.4}=0.25\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(\Rightarrow a+1.5b=0.25\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(\%Fe=\dfrac{5.6}{8.3}\cdot100\%=67.47\%\)
\(\%Al=32.53\%\)
bạn ơi cho mik hỏi: tại sao lại suy ra: a+1,5b=0,25 vậy ạ ? và cả bước tiếp theo nx ạ ?

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
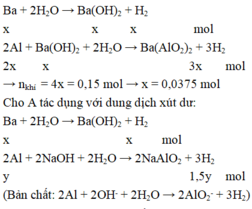

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

Đáp án B
Các phản ứng tạo kết tủa:
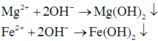
Dung dich X có ![]()
Dung dịch Y có ![]()
Mà ![]() nên OH-dư và
nên OH-dư và ![]()
Vậy ![]()

Đáp án B
nOH- = 2nH2 = 0,4
nCl- = 2nH2 = 0,3
m↓ = 5,2 + 0,3.17 = 10,3 g
mmuối = 5,2+0,3.35,5= 15,85 g
