Không dùng thuốc thử phân biệt dung dịch: NaCl, CuSO4, H2SO4, MgCl2, NaOH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án cần chọn là: A
- dùng dung dịch BaCl2, dung dịch AgNO3, quỳ tím
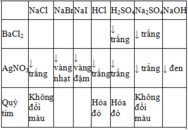

- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Không đổi màu: NaCl, MgCl2 và Na2SO4
- Đổ dd BaCl2 vào từng dd còn lại
+) Xuất hiện kết tủa trắng: Na2SO4
PTHH: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\downarrow\)
+) Không hiện tượng: NaCl và MgCl2
- Đổ dd KOH vào 2 dd còn lại
+) Xuất hiện kết tủa: MgCl2
PTHH: \(MgCl_2+2KOH\rightarrow2KCl+Mg\left(OH\right)_2\downarrow\)
+) Không hiện tượng: NaCl

- Dùng quỳ tím
+) Hóa đỏ: HCl
+) Không đổi màu: NaCl, MgCl2 và Na2SO4
- Đổ dd BaCl2 vào từng dd còn lại
+) Xuất hiện kết tủa trắng: Na2SO4
PTHH: BaCl2+Na2SO4→2NaCl+BaSO4↓
+) Không hiện tượng: NaCl và MgCl2
- Đổ dd KOH vào 2 dd còn lại
+) Xuất hiện kết tủa: MgCl2
PTHH: MgCl2+2KOH→2KCl+Mg(OH)2↓
+) Không hiện tượng: NaCl

trích mẫu thử rồi đổ các dd vào vs nhau ta đc bảng sau
| NaCl | CuSO4 | H2SO4 | MgCl2 | NaOH | |
| NaCl | - | - | - | - | - |
| CuSO4 | - | - | - | - | tủa xanh |
| H2SO4 | - | - | - | - | - |
| MgCl2 | - | - | - | - | tủa trắng |
| NaOH | - | tủa | - | tủa | - |
dd tạo rủa vs 2 dd => NaOH
dd tạo tủa trắng vs 1 dd => MgCl2
dd tạo tủa xanh vs 1 dd => CuSO4
còn : NaCl , H2SO4
lấy tủa thu đc ở pư trên là Mg(OH)2 cho vào 2dd còn lại
tủa bị hòa tan => H2SO4
còn lại NaCl
| NaOH | (NH4)2CO3 | BaCl2 | MgCl2 | H2SO4 | |
| NaOH | - | khí | - | tủa | - |
| (NH4)2CO3 | khí | - | tủa | tủa | khí |
| BaCl2 | - | tủa | - | - | tủa |
| MgCl2 | tủa | tủa | - | - | - |
| H2SO4 | - | khí | tủa | - | - |
dd tạo khí vs 2dd và tủa vs 2dd => (NH4)2CO3
nhóm A dd tạo 2 tủa vs 2 dd => MgCl2 , BaCl2
nhóm B dd tạo tủa vs 1 dd và khí vs 1 dd => NaOH , H2SO4
lấy tủa BaCO3 (thu đc ở pư của (NH4)2CO3 với BaCO3) cho vào nhóm B
dd nào hòa tan BaCO3 => H2SO4
còn lại NaOH
cho H2SO4 vào nhóm A
dd tạo tủa vs H2SO4 => BaCl2
còn lại MgCl2

Na2SO4 + BaCl2 → BaSO4 ↓ + 2NaCl
Trong khi NaCl + BaCl2 thì k0 có hiện tượng xảy ra.
- Thử với lượng nhỏ mỗi chất.
- Dùng quỳ tím cho vào các mẫu thử:
+) Qùy tím hóa đỏ -> Nhận biết: ddH2SO4.
+) Qùy tím không đổi màu -> Là 2 dd còn lai.
- Sau đó cho vài giọt dd BaCl2 vào 2dd chưa nhận biết được:
+) Xuất hiện kết tủa trắng -> Là BaSO4 => Nhận biết dd ban đầu là Na2SO4.
PTHH: BaCl2 + Na2SO4 -> BaSO4 (trắng) + 2 NaCl
+) Không xuất hiện kết tủa trắng => dd ban đầu là NaCl.

Dùng NaOH nhận biết được $AlCl_3$ do tạo kết tủa rồi kết tủa bị hòa tan, $MgCl_2$ do tạo kết tủa không tan và NaCl, $H_2SO_4$ không cho hiện tượng (Nhóm 1)
Lọc lấy $Mg(OH)_2$ đem hòa tan bởi nhóm 1. Chất hòa tan kết tủa là $H_2SO_4$, chất còn lại là $NaCl$
Trích mẫu thử
Cho dung dịch $Na_2CO_3$ vào mẫu thử
- mẫu thử nào tạo khí là $H_2SO_4$
$Na_2CO_3 + H_2SO_4 \to Na_2SO_4 + CO_2 + H_2O$
- mẫu thử nào tạo kết tủa trắng là $AlCl_3,MgCl_2$
$2AlCl_3 + 3Na_2CO_3 + 3H_2O \to 2Al(OH)_3 + 3CO_2 + 6NaCl$
$Na_2CO_3 + MgCl_2 \to MgCO_3 + 2NaCl$
- mẫu thử không hiện tượng là $NaCl$
Cho dung dịch $H_2SO_4$ nhận được vào hai kết tủa ở thí nghiệm trên
- mẫu thử nào tan, tạo khí là $MgCl_2$
$MgCO_3 + H_2SO_4 \to MgSO_4 + CO_2 + H_2O$
- mẫu thử tan là $AlCl_3$
$2Al(OH)_3 + 3H_2SO_4 \to Al_2(SO_4)_3 + 6H_2O$
Cho lần lượt các mẫu thử của các chất này tác dụng với nhau:
+ Chất nào cho phản ứng với các chất còn lại, không hiện tượng đó là NaCl và H2SO4.
+ Chất nào cho phản ứng với các chất còn lại, tạo 1 kết tủa trắng là MgCl2:
MgCl2 + 2NaOH -> Mg(OH)2↓ + 2NaCl
+ Chất nào cho phản ứng với các chất còn lại, tạo 1 kết tủa xanh là CuSO4:
CuSO4 + 2NaOH -> Cu(OH)2↓ + Na2SO4
+ Chất nào cho phản ứng với các chất còn lại, tạo 1 kết tủa trắng và 1 kết tủa xanh là NaOH:
2NaOH + MgCl2 -> Mg(OH)2↓ + 2NaCl
2NaOH + CuSO4 -> Cu(OH)2↓ + Na2SO4
-> Còn 2 chất chưa nhận biết được là NaCl và H2SO4. Đặt nó là nhóm A.
Nếu bạn để ý kĩ thì đề yêu cầu : không dùng thêm chất nào khác. Mình làm như sau.
Thu lấy 1 trong 2 kết tủa là Mg(OH)2 hay Cu(OH)2. Cho vào nhóm A:
-> Kết tủa tan trong chất nào thì chất đó là H2SO4:
Mg(OH)2 + H2SO4 -> MgSO4 + 2H2O
Cu(OH)2 + H2SO4 -> CuSO4 + 2H2O
-> Chất còn lại là NaCl.