Hỗn hợp B gồm các kim loại : K , Ba , Cu . Hòa tan 3,18 hỗn hợp B vào nước dư , sau khi phản ứng hoàn toàn thu được dung dịch C và m gam chất rắn D . Cô cạn dung dịch C thu được 3,39 gam chất rắn màu trắng . Đem chất rắn D nung trong không khí đến khối lượng không đổi thì được chất rắn E có khối lượng ( m+0,16 ) gam . Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp B .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chất rắn D là Cu, chất rắn E là CuO
\(m_{tăng}=m_{O_2}=0,16\left(g\right)\)
=> \(n_{O_2}=\dfrac{0,16}{32}=0,005\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
0,01<-0,005
=> mCu = 0,01.64 = 0,64 (g)
Gọi số mol K, Ba là a, b (mol)
=> 39a + 137b = 3,18 - 0,64 = 2,54 (1)
PTHH: 2K + 2H2O --> 2KOH + H2
a--------------->a
Ba + 2H2O --> Ba(OH)2 + H2
b--------------->b
=> 56a + 171b = 3,39 (2)
(1)(2) => a = 0,03 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,64}{3,18}.100\%=20,126\%\\\%m_K=\dfrac{0,03.,39}{3,18}.100\%=36,792\%\\\%m_{Ba}=\dfrac{0,01.137}{3,18}.100\%=43,082\%\end{matrix}\right.\)
\(m_{O_2}=m+0,16-m=0,16\left(g\right)\\ \rightarrow n_{O_2}=\dfrac{0,16}{32}=0,005\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
0,01 0,005
Gọi \(\left\{{}\begin{matrix}n_K=a\left(mol\right)\\n_{Ba}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
2K + 2H2O ---> 2KOH + H2
a a
Ba + 2H2O ---> Ba(OH)2 + H2
b b
Hệ pt \(\left\{{}\begin{matrix}39a+137b=3,18-0,01.64=2,54\\56a+171b=3,39\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,03\left(mol\right)\\b=0,01\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,01.64}{3,18}=20,13\%\\\%m_K=\dfrac{0,03.39}{3,18}=36,79\%\\\%m_{Ba}=100\%-20,13\%-36,79\%=43,08\%\end{matrix}\right.\)

Chọn đáp án C
Giả sử KOH tác dụng với X thì KOH hết ⇒ n KNO 3 = n KOH = 0 , 5 mol.
⇒ m KNO 3 = 0 , 5 x 101 = 50 , 5 gam gam > 41,05 gam ⇒ vô lí ⇒ KOH dư.
Đặt n KOH dư = x mol; n KNO 3 = y mol
![]()
Phản ứng:
![]()
Giải hệ có: x = 0,05 mol; y = 0,45 mol
![]()
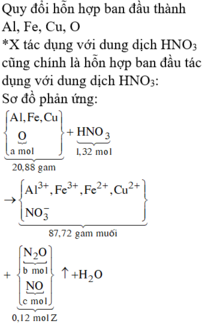
Đặt n Fe = a mol; n Cu = b mol ⇒ m A = 56 a + 64 b = 11 , 6 gam.
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.
![]()
⇒ dung dịch chứa ion Fe2+, Fe3+ và H+ hết.!
Bảo toàn nguyên tố hidro có n H 2 O = 0 , 7 ÷ 2 = 0 , 35 mol.
⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
![]()


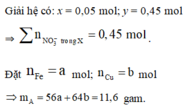
Do KOH dư ⇒ kết tủa hết ion kim loại ⇒ nung T thì rắn gồm Fe2O3 và CuO.
⇒ mrắn = 41,05 = 0,5a × 160 + 80b. Giải hệ có: a = 0,15 mol; b = 0,05 mol.
Quy hỗn hợp B về N và O. Bảo toàn nguyên tố nitơ có nN spk = 0,7 – 0,45 = 0,25 mol.

⇒ bảo toàn nguyên tố oxi có nO sk = 0,7 × 3 – 0,45 × 3 – 0,35 = 0,4 mol.
⇒ BTKL mdung dịch sau phản ứng = 11,6 + 87,5 – 0,25 × 14 – 0,4 × 16 = 89,2 gam.
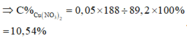
Đáp án C

B3:
Bài 3 người ta cho các kim loại sau đây là những kim loại nào thế?
B2:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\\ MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\\ Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+H_2O\\ Mg\left(OH\right)_2\rightarrow\left(t^o\right)MgO+H_2O\\ Đặt:n_{Al}=a\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}27a+24b=10\\40b=6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=\dfrac{32}{135}\\b=0,15\end{matrix}\right.\\ \Rightarrow\%m_{Mg}=\dfrac{0,15.24}{10}.100\%=36\%\)

a, \(Fe_3O_4+4H_2SO_4\rightarrow FeSO_4+Fe_2\left(SO_4\right)_3+4H_2O\) (1)
\(Cu+Fe_2\left(SO_4\right)_3\rightarrow CuSO_4+2FeSO_4\) (2)
\(Cu+2H_2SO_{4\left(đ\right)}\underrightarrow{t^o}CuSO_4+SO_2+2H_2O\) (3)
\(2Fe_3O_4+10H_2SO_{4\left(đ\right)}\underrightarrow{t^o}3Fe_2\left(SO_4\right)_3+SO_2+10H_2O\) (4)
\(5SO_2+2KMnO_4+2H_2O\rightarrow2MnSO_4+K_2SO_4+2H_2SO_4\) (5)
b, - K là Fe3O4 dư. → mFe3O4 (dư) = 0,4 (g)
- B gồm: CuSO4, FeSO4 và Fe2(SO4)3.
Gọi: số mol Cu, Fe3O4 pư với H2SO4 loãng lần lượt là: x, y (mol)
⇒ 64x + 232y = 8 - 0,4 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{FeSO_4\left(1\right)}=n_{Fe_2\left(SO_4\right)_3\left(1\right)}=n_{Fe_3O_4}=y\left(mol\right)\\n_{CuSO_4}=n_{Fe_2\left(SO_4\right)_3\left(2\right)}=n_{Cu}=x\left(mol\right)\\n_{FeSO_4\left(2\right)}=2n_{Cu}=2x\left(mol\right)\end{matrix}\right.\)
→ Trong B có: CuSO4: x (mol), FeSO4: y + 2x (mol) và Fe2(SO4)3: y - x (mol)
⇒ 160x + 152(y+2x) + 400(y-x) = 17,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
⇒ mCuSO4 = 0,01.160 =1,6 (g)
mFeSO4 = (0,03+2.0,01).152 = 7,6 (g)
mFe2(SO4)3 = (0,03-0,01).400 = 8 (g)
c, Trong 8 (g) hh có Cu: 0,01 (mol) và Fe3O4: 0,03 + 0,4/232 = 23/725 (mol)
Theo PT: \(n_{SO_2}=n_{Cu}+\dfrac{1}{2}n_{Fe_3O_4}\approx0,026\left(mol\right)\)
\(n_{KMnO_4}=0,04.1=0,04\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,026}{5}< \dfrac{0,04}{2}\), ta được KMnO4 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{KMnO_4\left(pư\right)}=n_{MnSO_4}=n_{H_2SO_4}=\dfrac{2}{5}n_{SO_2}=0,0104\left(mol\right)\\n_{K_2SO_4}=\dfrac{1}{5}n_{SO_2}=0,0052\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{KMnO_4\left(dư\right)}=0,04-0,0104=0,0296\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{KMnO_4}\left(dư\right)}=\dfrac{0,0296}{0,04}=0,74\left(M\right)\\C_{M_{MnSO_4}}=C_{M_{H_2SO_4}}=\dfrac{0,0104}{0,04}=0,26\left(M\right)\\C_{M_{K_2SO_4}}=\dfrac{0,0052}{0,04}=0,13\left(M\right)\end{matrix}\right.\)

Chất rắn B là Cu
mCu tăng= 0,16g= mO
=> nO= 0,16/16= 0,01 mol
Cu+ O -> CuO
=> nCu= 0,01 mol
=> mCu= 0,01.64= 0,64g
mFe,Al= 1,74-0,64= 1,1g
2Al+ 6HCl -> 2AlCl3+ 3H2
Fe+ 2HCl -> FeCl2+ H2
Đặt x là mol Al; y là mol Fe
Ta có hệ: 27x+ 56y= 1,1 và 133,5x+ 127y= 3,94
<=> x=0,02; y=0,01
=> mAl= 0,02.27= 0,54g
mCu= 0,01.64=0,64g
=> mFe=0,01.56=0,56 g


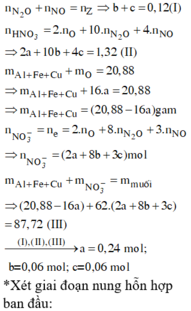
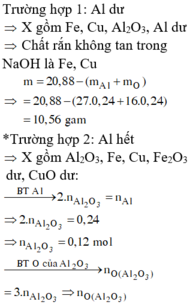
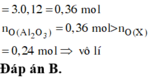

Hòa tan 3,18 gam hỗn hợp B vào nước dư thì chỉ có K, Ba tan hết còn Cu không tan.
PTHH:
2K + 2H2O —> 2KOH + H2
Ba + 2H2O —> Ba(OH)2 + H2
- Dung dịch C là: KOH, Ba(OH)2
- Chất rắn D là: Cu.
- Cô cạn dung dịch C thu được 3,39 gam.
=> mKOH + mBa(OH)2 = 3,39 gam.
- Đem D nung nóng trong không khí có:
PTHH : 2Cu + O2 —> 2CuO
mol 0,01 <— 0,005
Theo đề bài, ta có:
mCuO= m+0, 16 (gam)
=> mO2= 0,16 gam
=> nO2= m/M= 0,16/32= 0,005 mol.
Theo PTHH, ta có:
nCu= 2nO2= 2× 0,005=0, 01 mol.
=> mCu= n. M=0, 01.64= 0,64 gam.
=> m(K+Ba) =3,18-0, 64=2, 54 gam.
Đặt nK=x(mol), nBa= y(mol)
=> 39x+137y=2, 54(gam) (1)
Theo PTHH, ta có:
nKOH=nK=x(mol)
nBa(OH)2 = nBa=y(mol)
=> 56x+171y= 3,39 gam (2)
Từ (1), (2)
=> x= 0,03 hay nK=0, 03 mol
=> y= 0,01 hay nBa= 0,01 mol
=> % mK= 0,03.39/3, 18.100%
= 36,68%
% mBa= 0,01.137/3,18 . 100%
= 43,08%
=> % mCu = 100 -43, 08-36, 68
= 20,24%
sai