Cho m gam Na vào 100ml dung dịch HCl 0,2 M, thu được 0,336 lít khí H2(đktc) và 100ml dung dịch X. pH của dung dịch X là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Na + H2O ---> NaOH + 1/2H2;
x x x/2
NaOH + HCl ---> NaCl + H2O;
0,1 0,1
Dung dịch X gồm NaCl và NaOH dư;
Số mol NaOH dư = x - 0,1 mol; lượng NaOH dư được trung hòa bằng 0,02 mol HCl nên: x - 0,1 = 0,02 hay x = 0,12 mol.
Vậy: m = 23.0,12 = 2,76 g; V = 0,06.22,4 = 1,344 lít.

Chọn đáp án B
Chú ý : Khi cho HCl vào C O 3 2 - thì
![]()
Nhưng khi cho C O 3 2 - vào HCl thì
![]()
+ Ta có :
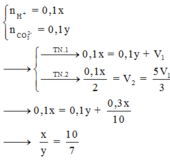

Đáp án D
2H+ +CO32- →CO2+ H2O
0,1← 0,1
Ba2++ CO32- →BaCO3
0,1→ 0,1
Ba2++ SO42- →BaSO4
0,1 ← (43-0,1.197)/233
NH4++ OH- →NH3+ H2O
0,2← 0,2
Áp dụng ĐLTBT ĐT có: 1.nNa++ 0,2.1=0,1.2+0,1.2 suy ra nNa+= 0,2 mol
tổng khối lượng muối có trong 500ml dung dịch X là: (0,2.23+0,1.60+0,1.96+0,2.18).5= 119 gam

Đáp án B
nFeCl2 = nH2 = 0,1mol; nKMnO4 = 0,025 mol
Fe2+ sẽ phản ứng trước với KMnO4 / H+, mà thu được khí clo nên Fe2+ đã phản ứng hết, tiếp là Cl-
Bảo toàn e: nFe2+ + nCl- (pư) = 5.nMn+7
⇒ nCl- (pư) = 0,025 .5 – 0,1 = 0,025
nFe2+ + nCl- (pư) = 5.nMn7+ ⇒ nCl- (pư) = 0,025 .5 – 0,1 = 0,025 mol
⇒ nCl2 = 0,0125 mol ⇒ VCl2 = 0,28l
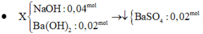

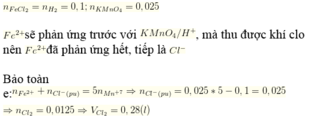
\(n_{HCl}=0,2\cdot0,1=0,02mol\\ n_{H_2}=\dfrac{0,336}{22,4}=0,015mol\\ 2Na+2HCl\rightarrow2NaCl+H_2\uparrow\)
0,02 > 0,015
\(n_{HCldư}=0,02-0,015=5\cdot10^{-3}mol\\C_{M_X}=\dfrac{5\cdot10^{-3}}{0,1}=0,05M\)
\(\Rightarrow pH=1,3\)