Đốt cháy hoàn toàn 4 gam 1 este đơn chức thu được 4,48 lít CO2 (đktc) và 2,88 gam nước. Tìm CTPT của este.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án: C
Giả sử công thức este là CnH2nO2
⇒
4
,
4
n
14
n
+
32
=
n
C
O
2
=
0
,
2
⇒
n
=
4
⇒
C
4
H
8
O
2

Giải thích:
nCO2 = 0,2 (mol) ; nH2O = 0,2 (mol) => este no, đơn chức
Gọi CTPT của este là CnH2nO2
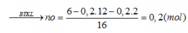
=> neste = 1/2 nO = 0,1 (mol)
=> Meste = 6/ 0,1 = 60
=> 14n + 32 = 60 => n = 2
Vậy CTPT của este là C2H4O2
Đáp án B

Đáp án: C
Do đốt este no đơn chức nên
n
C
O
2
=
n
H
2
O
=
0
,
12
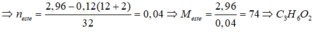

Đáp án D
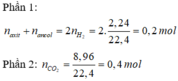
Phần 3:
0,11g este + O 2 → 0,005 mol CO 2 +0,005mol H 2 O
Þ Este no Þ Axit và ancol đều no.
Áp dụng định luật bảo toàn khối lượng có:
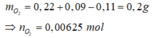
Áp dụng định luật bảo toàn nguyên tố O có: 2neste=2.0,005 + 0,005 – 2.0,00625=0,0025 mol Þ neste= 0,00125 mol
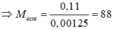
Þ CTPT của este là C4H8O2
Trường hợp 1: Axit là HCOOH (a mol) , ancol là C3H7OH (b mol)
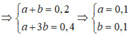
Trường hợp 2: Axit CH3COOH ( a mol), ancol là C2H5OH (b mol)
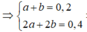
Thỏa mãn với tất cả các giá trị 0 < a, b<0,2
Trường hợp 3: Axit C2H5COOH (a mol), ancol là CH3OH (b mol)
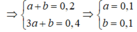
Vậy cả 3 trường hợp đều thỏa mãn.

Ta có:
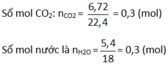
Vì nCO2 = nH2O ⇒ X là este no đơn chức mạch hở. Gọi CTPT của este X là CnH2nO2

⇔ 3(14n + 32) = 74n ⇒ n = 3
⇒ Công thức phân tử của este X là C3H6O2
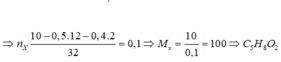
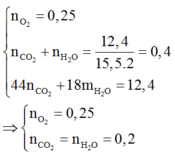
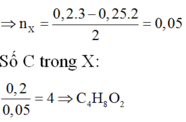
$n_{CO_2} = 0,2(mol) ; n_{H_2O} = 0,16(mol)$
Bảo toàn C,H :
$n_C = n_{CO_2} = 0,2(mol)$
$n_H = 2n_{H_2O} = 0,32(mol)$
$\Rightarrow n_O = \dfrac{4 - 0,2.12 - 0,32}{16} = 0,08(mol)$
Ta có :
$n_C : n_H : n_O = 0,2 : 0,32 : 0,08 = 4:8 :2$
Vậy CTPT là $C_4H_8O_2$
este là chất ak bn