cho 9,6 gam kim loại Mg vào 120 gam dung dịch HCl nồng độ phần trăm của dung dịch sau phản ứng là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
PTHH: Mg + 2HCl → MgCl2 + H2
Mol: 0,2 0,4 0,2 0,2
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b,\(C\%_{ddHCl}=\dfrac{0,4.36,5.100\%}{200}=7,3\%\)
c, mdd sau pứ = 4,8+200-0,2.2 = 204,4 (g)
\(C\%_{ddMgCl_2}=\dfrac{0,2.95.100\%}{204,4}=9,3\%\)

\(CT:ACO_3\)
\(n_{CO_2}=\dfrac{4.4912}{22.4}=0.2005\left(mol\right)\)
\(ACO_3+2HCl\rightarrow ACl_2+CO_2+H_2O\)
\(0.2005.....0.401.....0.2005...0.2005\)
\(M_{ACO_3}=\dfrac{20.05}{0.2005}=100\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow A=100-60=40\)
\(A:Ca\left(Canxi\right)\)
\(m_{CaCl_2}=0.2005\cdot111=22.2555\left(g\right)\)
\(m_{dd}=20.05+100-0.2005\cdot44=111.228\left(g\right)\)
\(C\%_{CaCl_2}=\dfrac{22.2555}{111.228}\cdot100\%=20\%\)

PTHH: \(2M+2xHCl\rightarrow2MCl_x+xH_2\uparrow\) (x là hóa trị của M)
Tính theo sản phẩm
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow n_M=\dfrac{0,4}{x}\left(mol\right)\) \(\Rightarrow M=\dfrac{4,8}{\dfrac{0,4}{x}}=12x\)
Ta thấy với \(x=2\) thì \(M=24\) (Magie)
Mặt khác: \(n_{HCl}=\dfrac{50\cdot36,5\%}{36,5}=0,5\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{MgCl_2}=n_{H_2}=0,2\left(mol\right)\\n_{HCl\left(dư\right)}=0,1\left(mol\right)\end{matrix}\right.\)
Ta lại có: \(m_{dd\left(sau.p/ứ\right)}=m_{Mg}+m_{ddHCl}-m_{H_2}=4,8+50-0,2\cdot2=54,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{0,2\cdot95}{54,4}\cdot100\%\approx34,93\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1\cdot36,5}{54,4}\cdot100\%\approx6,71\%\end{matrix}\right.\)

1.
nAl=\(\dfrac{5,4}{27}\)=0,2 mol
mHCl=\(\dfrac{175.14,6}{100}\)=25,55g
nHCl=\(\dfrac{25,55}{36,5}\)=0,7
2Al + 6HCl → 2AlCl3 + 3H2↑
n trước pứ 0,2 0,7
n pứ 0,2 →0,6 → 0,2 → 0,3 mol
n sau pứ hết dư 0,1
Sau pứ HCl dư.
mHCl (dư)= 36,5.0,1=3,65g
mcác chất sau pư= 5,4 +175 - 0,3.2= 179,8g
mAlCl3= 133,5.0,2=26,7g
C%ddHCl (dư)= \(\dfrac{3,65.100}{179,8}=2,03%\)%
C%ddAlCl3 = \(\dfrac{26,7.100}{179,8}\)= 14,85%
2.
200ml= 0,2l
mMg= \(\dfrac{4,2}{24}=0,175mol\)
Mg + 2HCl → MgCl2 + H2↑
0,175→ 0,35 → 0,175→0,175 mol
a) VH2= 0,175.22,4=3,92l.
b)C%dHCl= \(\dfrac{0,35}{0,2}=1,75\)M

Đáp án A
Gọi n là hoá trị của M; x là số mol của M
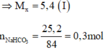
Phương trình hoá học:
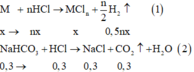
Dung dịch X thu được gồm NaCl: 0,3 mol; MCn: x mol; HCl dư

Tổ hợp (I) và (II) ta được:
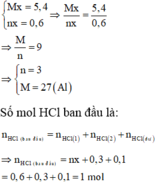
Số mol các khí thu được theo (1), (2) là:
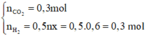
Nồng độ phần trăm của NaCl trong dung dịch X là:
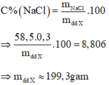
Mặt khác, ta có:
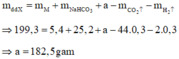
Nồng độ phần trăm dung dịch HCl ban đầu là:
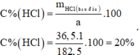


nMg=9.6/24=0.4mol
Mg + 2HCl -> MgCl2 + H2
(mol) 0.4 0.4 0.4
mMgCl2=0.4*95=38g
mdd=mMg + mddHCl - mH2= 9.6+120-0.4*2=128.8g
C%MgCl2=38/128.8*100=29.5%
mdd= mMG + mddHCl - mH2 = 9,6 + 120 - 0,4*2 = 128,8
cho mình hỏi 0,4 đó là mol hay là gam của H2 ạ ?