Để pha chế 300 ml dung dịch H2SO4 0,5M người ta trộn dung dịch H2SO4 1,5M với dung dịch H2SO4 0,3M. Tính thể tích mỗi dung dịch cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nH2SO4 cần pha = CM. V = 0,5 . 0,3 = 0,15(mol)
Gọi V1 là thể tích dd H2SO4 1,5M
Gọi V2 là thể tích dd H2SO4 0,5M
Ta có: V1 + V2 = 0,3
1,5V1 + 0,3V2 = 0,15
=> V1 = 0,05
V2 = 0,25

a) mM (1)= 200*20/100= 40g
mM (2)= 300*5/100=15g
mM= 40+15=55g
mdd= 200+300=500g
C%= 55/500*100%= 11%
b) Đặt: VH2SO4 (1)= x (l)
VH2SO4 (2)= y (l)
nH2SO4 (1)= 1.5x mol
nH2SO4 (2)= 0.3y mol
nH2SO4= 1.5x + 0.3y= 0.3*0.5=0.15 (mol) (1)
VH2SO4= x + y = 0.3 l (2)
Giải (1) và (2):
x= 0.05
y= 0.25
VH2SO4 (1)= 0.05l
VH2SO4 (2)= 0.25l

Áp dụng sơ đồ đường chéo ta có:
\(\dfrac{V_{H_2SO_4\left(0,3M\right)}}{V_{H_2SO_4\left(1,5M\right)}}=\dfrac{0,5-0,3}{1,5-0,5}=\dfrac{0,2}{1}=0,2\\ \Rightarrow V_{H_2SO_4\left(0,3M\right)}=0,2.V_{H_2SO_4\left(1,5M\right)}\)
Mà \(V_{H_2SO_4\left(0,3M\right)}+V_{H_2SO_4\left(1,5M\right)}=0,3\left(l\right)\)
Thay vào ta được:
\(0,2.V_{H_2SO_4\left(1,5M\right)}+V_{H_2SO_4\left(1,5M\right)}=0,3\\ \Rightarrow V_{H_2SO_4\left(1,5M\right)}=0,1\left(l\right)\\ \Rightarrow V_{H_2SO_4\left(0,3M\right)}=0,2\left(l\right)\)
Vậy.....................
- ta có:
\(\dfrac{V_1}{V_2}\) = \(\dfrac{C_2-C}{C-C_1}\)<=> \(\dfrac{V_1}{0,3-V_1}\)= \(\dfrac{1,5-0,5}{0,5-0,3}\)
=>V1 = 0,25 (l)
=>V2 = 0,3 - 0,25 = 0,05 (l)

1. \(n_{H_2SO_4\left(98\%\right)}=\dfrac{30.1,84.98\%}{98}=0,552\left(mol\right)\)
=>\(V_{H_2SO_4\left(1M\right)}=\dfrac{0,552}{1}=0,552\left(l\right)\)

Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên: 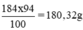
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất: 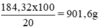
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.

Chọn đáp án D
Cần thật thật chú ý là trộn 3 thể tích bằng nhau các dung dịch
⇒ tạo 300 ml dung dịch X gồm 100 mL HCl 0,3M; 100 mL H2SO4 0,2M và 100 mL H3PO4 0,1M ||⇒
![]() mol.
mol.
V mL dung dịch Y gồm 2x mol NaOH và x mol Ba(OH)2
⇒ ![]() x mol.
x mol.
Phản ứng trung hòa:
![]()
⇒ 4x = 0,1 ⇒ x = 0,025 mol ⇒ V = n ÷ CM = 0,025 ÷ 0,1 = 0,25 lít ⇔ 250 mL.
⇒ chọn đáp án D.

Đáp án A
nH+= nHCl+ 2nH2SO4+ 3nH3PO4= 0,1.0,3+ 2.0,2.0,1+ 3.0,1.0,1=0,1 mol
nOH-= (V.0,1+2.0,2.V)/1000 mol
H+ + OH-→ H2O
Theo PT: nH+= nOH- nên 0,1=(V.0,1+2.0,2.V)/1000 suy ra V= 200 ml

\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{0,2}=5\)
\(\Rightarrow V_1=5V_2\)
Mà \(V_1+V_2=0,3\)
\(\Rightarrow\left\{{}\begin{matrix}V_1=0,05\left(l\right)\\V_2=0,25\left(l\right)\end{matrix}\right.\)