Cho 4,48l CO ở đktc đi từ từ qua ống sứ nung nóng đựng 8g một oxit sắt đến khi phản ứng xảy ra hoàn toàn. Hỗn hợp khí thu được sau phản ứng có tỉ khối so với hidro =20. Tính công thức của oxit sắt l=và tinh % thể tích của CO2 trong hỗn hợp sau phản ứng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cho hỏi chỗ sơ đồ đường chéo 4 và 12 là như nào đấy ạ .___.
Còn cả chỗ suy ra 42x-28y=0

Đáp án B
Đặt công thức oxit sắt là FexOy có số mol là a mol
Ta có: nCO= 0,2 mol
FexOy+ yCO → t 0 xFe + yCO2
a ay ax ay mol
Sau phản ứng thu được ay mol CO2, (0,2-ay) mol CO dư
M ¯ = m h h n h h = 44 . a y + 28 . ( 0 , 2 - a y ) a y + 0 , 2 - a y = 40 → a y = 0 , 15 m o l T a c ó : m F e x O y = a ( 56 x + 16 y ) = 56 a x + 16 a y = 8 g a m → a x = 0 , 1 m o l → x y = a x a y = 0 , 1 0 , 15 = 2 3 → C ô n g t h ứ c o x i t l à F e 2 O 3
Sau phản ứng thu được 0,15 mol C O 2 và 0,05 mol CO dư
→ % V C O 2 = 0 , 15 0 , 2 . 100 % = 75 %

Ta có: nCO = 0,2 (mol)
- Hỗn hợp khí sau pư gồm: CO dư và CO2.
Gọi: \(\left\{{}\begin{matrix}n_{CO\left(pư\right)}=x\left(mol\right)\\n_{CO\left(dư\right)}=y\left(mol\right)\end{matrix}\right.\) ⇒ x + y = 0,2 (1)
\(CO_{\left(pư\right)}+O_{\left(trongoxit\right)}\rightarrow CO_2\)
x________x__________x (mol)
\(\Rightarrow\dfrac{44x+28y}{x+y}=20.2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
⇒ nO (trong oxit) = 0,15 (mol)
⇒ nFe (trong oxit) = 8 - 0,15.16 = 5,6 (g) ⇒ nFe = 0,1 (mol)
Gọi CTHH của oxit là FexOy.
\(\Rightarrow\dfrac{x}{y}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\)
Vậy: CTHH cần tìm là Fe2O3.
Gọi CTHH của oxit là $R_2O_n$
$R_2O_n + nCO \xrightarrow{t^o} 2R + nCO_2$
Hỗn hợp khí sau phản ứng gồm $CO$ dư (a mol) và $CO_2(b\ mol)$
Suy ra :
$a + b = \dfrac{4,48}{22,4} = 0,2$
$\dfrac{28a + 44b}{a + b} = 20.2$
Suy ra : a = 0,05 ; b = 0,15
Theo PTHH : $n_{oxit} = \dfrac{n_{CO_2}}{n} = \dfrac{0,15}{n}(mol)$
$\Rightarrow \dfrac{0,15}{n}.(2R + 16n) = 8$
$\Rightarrow R = \dfrac{56}{3}n$
Với n = 3 thì R = 56(Fe)
Vậy oxit là $Fe_2O_3$

Đáp án D
![]()
n O t r o n g a x i t p h ả n ứ n g = n C O p h ả n ứ n g = n C O 2 sin h r a => tổng số mol khí trước và sau phản ứng là không đổi.
Hỗn hợp khí sau khi phản ứng là CO2 và CO dư
![]()
![]()
n O t r o n g o x i t p h ả n ứ n g = 0 , 75 . 0 , 24 = 0 , 18
n F e = (10,44 - 0,18.16)/56 = 0,135 mol
Gọi công thức của oxit là F e x O y
Ta có: x:y = 0,135:0,18 = 3:4 => Công thức của oxit là Fe3O4

Đáp án D
MxOy + yCO ——> xM + yCO2
![]()
=> Tổng số mol khí trước và sau phản ứng là không đổi.
Hỗn hợp khí sau phản ứng là CO2 và CO dư
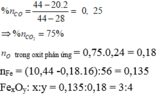

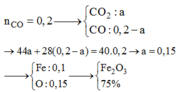
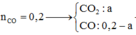
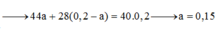
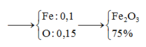



Gọi CTTQ: FexOy
......x (mol) là số mol CO pứ
Hóa trị của Fe: 2y/x
nCO2 bđ = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt: FexOy + yCO --to--> xFe + yCO2
.........\(\dfrac{x}{y}\)<------x-------------------> x
Mhh khí = 20 . 2 = 40
Ta có: \(\dfrac{44x+\left(0,2-x\right).28}{x+0,2-x}=40\)
=> x = 0,15
% VCO2 = \(\dfrac{0,15}{0,2}.100\%=75\%\)
% VCO = 100% - 75% = 25%
Ta có: \(8=\dfrac{0,15}{y}.\left(56x+16y\right)\)
\(\Leftrightarrow8=\dfrac{8,4x}{y}+2,4\)
\(\Leftrightarrow8,4x=5,6y\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{5,6}{8,4}=\dfrac{2}{3}\)
Vậy CTHH: Fe2O3