Làm thế nào để pha chế 250 g dung dịch h2so4 nồng độ 10% từ dung dịch h2so4 nồng độ 49%
( Mình đang cần gấp mong mọi người giúp đỡ ạ )
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có :
PTHH :
Na2O\(\left(\dfrac{x}{62}\right)\) + H2O\(\left(\dfrac{x}{62}\right)\) -----> 2NaOH\(\left(\dfrac{x}{31}\right)\)
Gọi x là số gam Na2O cần thêm
=> nNaOH = \(\left(\dfrac{x}{31}\right)\)
=> mNaOH = \(\dfrac{40x}{31}\)
Ta có :
200g dung dịch NaOH 2,5% => mNaOH(BĐ) = 5(g)
=> mNaOH sau khi thêm là : \(\dfrac{40x}{31}\)+5
=> mdd(NaOH) = 200 + \(\dfrac{40x}{31}\)
=> \(\dfrac{\left(\dfrac{40x}{31}+5\right)}{\left(200+\dfrac{40x}{31}\right)}=\dfrac{10}{100}\)
=> \(\dfrac{4000x}{31}+500=2000+\dfrac{400x}{31}\)
=> \(\dfrac{3600x}{31}=1500\Rightarrow x=12,92\left(g\right)\)
Vậy cần phải thêm 12,92(g) Na2O để được dung dịch NaOH 10%
Gọi x(lít) là VH2SO4(3M)
Gọi y(lít) là VH2SO4(1M)
Ta có :
x + y = 5
3x + y = 10
=> 2x = 5
=> x = 2,5(lít)
=> y = 2,5(lít)

a) mM (1)= 200*20/100= 40g
mM (2)= 300*5/100=15g
mM= 40+15=55g
mdd= 200+300=500g
C%= 55/500*100%= 11%
b) Đặt: VH2SO4 (1)= x (l)
VH2SO4 (2)= y (l)
nH2SO4 (1)= 1.5x mol
nH2SO4 (2)= 0.3y mol
nH2SO4= 1.5x + 0.3y= 0.3*0.5=0.15 (mol) (1)
VH2SO4= x + y = 0.3 l (2)
Giải (1) và (2):
x= 0.05
y= 0.25
VH2SO4 (1)= 0.05l
VH2SO4 (2)= 0.25l

\(n_{SO_3}=\dfrac{32}{80}=0.4\left(mol\right)\)
\(m_{H_2SO_4}=200\cdot10\%=20\left(g\right)\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(0.4.....................0.4\)
\(m_{dd}=32+200=232\left(g\right)\)
\(C\%H_2SO_4=\dfrac{0.4\cdot98+20}{232}\cdot100\%=25.57\%\)

\(\text{Giả sử có 1 mol MO: }\\ MO+H_2SO_4 \to MSO_4+H_2O\\ m_{ddH_2SO_4}=\frac{98.100}{20}=490(g)\\ C\%_{MSO_4}=\frac{M+96}{M+16+490}.100\%=22,64\%\\ \to M=24(Mg)\\ \to MgO\)

\(n_{Na_2O}=\dfrac{6,2}{62}=0,1 \left(mol\right)\)
\(2Na+2H_2O\rightarrow2NaOH+H_2\)
0,1 -----------------> 0,1
\(CM_{base}=CM_{NaOH}=\dfrac{0,1}{0,2}=0,5M\)
b
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
0,05 <------ 0,1
\(V_{H_2SO_4}=\dfrac{0,05}{0,2}=0,25\left(l\right)\Rightarrow V_{dd.H_2SO_4}=\dfrac{0,25.100}{20}=1,25\left(l\right)\)

Pha chế 50ml dung dịch H 2 S O 4 1,5M.
- Số mol H 2 S O 4 cần pha chế 50ml dung dịch H 2 S O 4 1,5M:
n H 2 S O 4 = CM.V = 1,5.0,05 = 0,075 (mol)
Gọi x(ml) là thể tích của dung dịch H 2 S O 4 1M (1)
Gọi y(ml) là thể tích của dung dịch H 2 S O 4 3M (2)
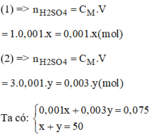
Giải hệ phương trình ta có: x = 37,5ml; y = 12,5ml
- Cách pha chế:
+ Đong lấy 37,5ml dung dịch H 2 S O 4 1M và 12,5ml dung dịch H 2 S O 4 3M cho vào bình, lắc đều, ta được 50ml dung dịch H 2 S O 4 1,5M.

- Giả sử có 100 gam dd H2SO4 98%
\(m_{H_2SO_4}=\dfrac{100.98}{100}=98\left(g\right)\) => \(n_{H_2SO_4}=\dfrac{98}{98}=1\left(mol\right)\)
\(V_{dd.H_2SO_4.98\%}=\dfrac{100}{1,84}=\dfrac{1250}{23}\left(ml\right)=\dfrac{5}{92}\left(l\right)\)
\(C_{M\left(dd.H_2SO_4.98\%\right)}=\dfrac{1}{\dfrac{5}{92}}=18,4M\)
-
\(n_{H_2SO_4}=18,4.0,05=0,92\left(mol\right)\)
=> \(m_{H_2SO_4}=0,92.98=90,16\left(g\right)\)
=> \(m_{dd.H_2SO_4.10\%}=\dfrac{90,16.100}{10}=901,6\left(g\right)\)
*Phần tính toán:
Khối lượng H2SO4 có trong 250g dd H2SO4 10%:
mH2SO4= \(\dfrac{m_{dd}.C\%}{100\%}\)=\(\dfrac{250.10}{100}\)= 25 (g)
Khối lượng dd H2SO4 49% cần lấy:
m'dd = \(\dfrac{m_{ct}.100\%}{C'\%}\)=\(\dfrac{25.100}{49}\)≃ 51 (g)
=> mH2O = 250 - 51 = 199 (g)
*Phần pha chế:
- Cân khoảng 51g dd H2SO4 49% vào cốc có dung tích 500ml.
- Đong 199ml nước cất (≃ 199g) cho vào cốc trên.
- Khuấy đều, ta được 250g dd H2SO4 10%.