cần bao nhiêu gam Ba(OH)2 để pha chế 250ml dung dịch có pH =11
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
[OH-]= 10-3 (M), nOH-= 0,25.10-3=2,5.10-4 (mol)
Ba(OH)2 → Ba2+ + 2OH-
1,25.10-4 mol 2,5.10-4 mol
mBa(OH)2= 1,25.10-4.171=0,021375 gam

Gọi: mBa(OH)2 thêm vào = a (g)
Ta có: \(m_{Ba\left(OH\right)_2\left(bđ\right)}=800.5\%=40\left(g\right)\)
\(\Rightarrow\dfrac{a+40}{a+800}=0,12\)
\(\Rightarrow a\approx63,64\left(g\right)\)

Khi pH = 10 thì [H+] = 1.10-10M và
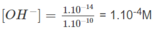
nghĩa là cần có 1. 10 - 4 mol NaOH trong 1 lít dung dịch.
Vậy trong 250 ml (0,25 lít) dung dịch cần có 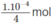 NaOH hoà tan, nghĩa là cần có
NaOH hoà tan, nghĩa là cần có
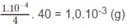 NaOH
NaOH

\(pH=14+log\left[OH^-\right]=10\)
\(\Rightarrow\left[OH^-\right]=10^{-4}\)
\(n_{NaOH}=10^{-4}\cdot0.3=3\cdot10^{-5}\left(mol\right)\)
\(m_{NaOH}=3\cdot10^{-5}\cdot40=1.2\cdot10^{-3}\left(g\right)\)

số mol Na2CO3 cần pha chế: 0,25*0,5=0,125mol
=> VddNa2CO3 ban đầu(2,5M)=0,125/2,5=0,05l=50ml
Vậy thể tích H2O cần thêm là 250-50=200ml
để pha chế 250ml dung dịch na2co3 0,5m từ dung dịch na2co3 2,5m người ta cần thêm bao nhiêu ml nước. pn jup mk thêm nha

Theo đề bài ta có
Số mol của NaOH hòa tan trong 250 ml dd NaOH 0,5M là
nNaOH=CM.V=0,5.0,25=0,125 mol
⇒⇒ Thể tích dung dịch NaOH 2M trong đó có chứa 0,125 mol NaOH là
\(v=\frac{n}{CM}=\frac{0,125}{2}=0,0625l=6,25ml\)

Số gam chất tan cần dùng để pha chế các dung dịch:
a) nNaCl = CM .V = 2,5.0,9 = 2,25 (mol)
→ mNaCl = 2,25.(23 + 35,5) = 131,625 (g)
b) 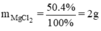
c) nMgSO4 = 0,1.0,25 = 0,025 (mol)
→ mMgSO4 = 0,025.(24 + 64 + 32) = 3 (g)