để hòa tan hết 31.05g hỗn hợp oxit gồm Zno và Feo thì cần vừa đủ V(ml) dung dich h2so4 2M. cô cạn dung dịch sau phản ứng thu được 63.05g muối khan. xác định V dung dịch H2so4 đem dùng.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 6 :
Bảo toàn nguyên tố H :
$n_{H_2O} = n_{H_2SO_4} =1,6.0,5 = 0,8(mol)$
Bảo toàn khối lượng :
$m = 107,4 + 0,8.18 - 0,8.98 = 43,4(gam)$
Bài 7 :
$Ba(OH)_2 + 2HCl \to BaCl_2 + 2H_2O$
$Ba(OH)_2 + H_2SO_4 \to BaSO_4 + 2H_2O$
$n_{HCl} = 0,001V(mol) ; n_{H_2SO_4} = 5.10^{-4}V(mol)$
Theo PTHH :
$n_{Ba(OH)_2} = \dfrac{0,001}{2} + 5.10^{-4}V = 10^{-3}V = 0,2$
$\Rightarrow V = 200(ml)$
$n_{BaSO_4} = n_{H_2SO_4} = 0,1(mol)$
$m = 0,1.233 = 23,3(gam)$
b)
$n_{BaCl_2} = \dfrac{1}{2}n_{HCl} = 0,1(mol)$
$m_{BaCl_2} = 0,1.208 = 20,8(gam)$
Câu 8 :
$n_{HCl} = 0,3(mol)$
$HCl + NaOH \to NaCl + H_2O$
$n_{HCl\ dư} = n_{NaOH} = 0,06(mol)$
$\Rightarrow n_{HCl\ pư} = 0,3 - 0,06 = 0,24(mol)$
Gọi n hóa trị của X
$2X + 2nHCl \to 2XCl_n + nH_2$
Theo PTHH :
$n_X = \dfrac{1}{n}.n_{HCl} = \dfrac{0,24}{n}(mol)$
$\Rightarrow \dfrac{0,24}{n}.X = 2,88 \Rightarrow X = 12n$
Với n = 2 thì $X = 24(Magie)$

\(\left\{{}\begin{matrix}n_{HCl}=0,2.4=0,8\left(mol\right)\\n_{HBr}=0,2.2=0,4\left(mol\right)\end{matrix}\right.\)
=> \(n_{H_2O}=0,6\left(mol\right)\)
=> nO = 0,6 (mol)
=> mkim loại = 34,8 - 0,6.16 = 25,2 (g)
=> mmuối = 25,2 + 0,8.35,5 + 0,4.80 = 85,6 (g)

1.
Đặt nFeO = x (mol); nZnO = y (mol); ( x, y > 0 )
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O (1)
ZnO + H2SO4 \(\rightarrow\) ZnSO4 + H2O (2)
Từ (1)(2) ta có hệ pt
\(\left\{{}\begin{matrix}72x+81y=31,05\\152x+161y=63,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,15\\y=0,25\end{matrix}\right.\)
\(\Rightarrow\) VH2SO4 = \(\dfrac{0,15+0,25}{2}\) = 0,2 (l)
nSO2 = 0,25 mol
ZnO +2HCl \(\rightarrow\) ZnCl2 + H2O (1)
Cu + 2H2SO4 đặc \(\underrightarrow{t^o}\) CuSO4 + SO2 + H2O (2)
Từ (2)
\(\Rightarrow\) %Cu = \(\dfrac{0,25.64.100}{40}\) = 40%
\(\Rightarrow\)%ZnO = 100% - 40% = 60%

Chọn A
Cần nhớ phản ứng cho oxit bazơ tác dụng với H 2 S O 4 thì:


Đáp án C
nH2O = nH2SO4 = 0,05 mol
BTKL: m muối = moxit + mH2SO4 – mH2O = 2,81 + 0,05.98 – 0,05.18 = 6,81 gam

nH2O = nH2SO4 = 0,05 mol
BTKL: m muối = moxit + mH2SO4 – mH2O = 2,81 + 0,05.98 – 0,05.18 = 6,81 gam
Đáp án C

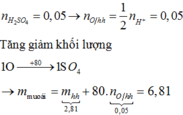
Đặt nZnO = x (mol); nFeO = y (mol); ( x, y > 0 )
ZnO + H2SO4 \(\rightarrow\) ZnSO4 + H2O (1)
FeO + H2SO4 \(\rightarrow\) FeSO4 + H2O (2)
Từ (1)(2) ta có hệ pt
\(\left\{{}\begin{matrix}81x+72y=31,05\\161x+152y=63,05\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}x=0,25\\y=0,15\end{matrix}\right.\)
\(\Rightarrow\) V H2SO4 = \(\dfrac{0,25+0,15}{2}\) = 0,2 (l)
PTHH:
ZnO + H2SO4 -> ZnSO4 + H2O (1)
.x..........x...............x...........x.
FeO + H2SO4 -> FeSO4 + H2O (2)
.y..........y..............y...........y..
Ta có hệ pt \(\left\{{}\begin{matrix}81x+72y=31,05\\161x+152y=63,05\end{matrix}\right.\)
Giải hệ pt ta có \(\left\{{}\begin{matrix}x=0,25\\y=0,15\end{matrix}\right.\)
VH2SO4 ở (1) là: \(\dfrac{0,25}{2}\) = 0,125 (lit)
VH2SO4 ở (2) là \(\dfrac{0,15}{2}\)= 0,075 (lit)
=> VH2SO4 đem dùng là : 0,125 + 0,075 = 0,2 (lit) = 200 (ml)