cho 0,032 mol CO2 vào dung dịch X có hòa tan 0,02 mol KOH và 0,1 mol Ca(OH)2. Tính khối lượng kết tủa thu được biết các phản ứng xảy ra hoàn toàn
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
nOH- = 0,1.2 + 0,225 + 0,2 = 0,625 mol
Do nH+>nCO2 nên X có cả CO32- => X không có Ba2+ => nBaCO3 = 0,1 mol
Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+
x+y = nCO2 = 0,25
2x+y = nH+ = 0,35
=> x = 0,1; y = 0,15
Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol)
BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3
BTNT C: nCO2 ban đầu = nBaCO3 + nCO32- + nHCO3- = 0,1 + 0,13 + 0,195 = 0,425 mol
=> V = 9,52 lít

Đáp án A
nOH- = 0,1.2 + 0,225 + 0,2 = 0,625 mol
Do nH+>nCO2 nên X có cả CO32- => X không có Ba2+ => nBaCO3 = 0,1 mol
Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+
x+y = nCO2 = 0,25
2x+y = nH+ = 0,35
=> x = 0,1; y = 0,15
Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol)
BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3
BTNT C: nCO2 ban đầu = nBaCO3 + nCO32- + nHCO3- = 0,1 + 0,13 + 0,195 = 0,425 mol
=> V = 9,52 lít

Định hướng tư duy giải
Từ các đáp án → dung dịch chỉ có K+ và Na+
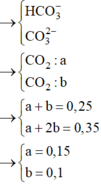
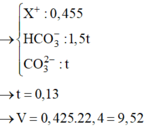

Đáp án A
nOH- = 0,1.2 + 0,225 + 0,2 = 0,625 mol
Do nH+>nCO2 nên X có cả CO32- => X không có Ba2+ => nBaCO3 = 0,1 mol
Đặt x, y là số mol CO32- và số mol HCO3- phản ứng với H+
x+y = nCO2 = 0,25
2x+y = nH+ = 0,35
=> x = 0,1; y = 0,15
Dung dịch X chứa: K+ (0,225 mol), Na+ (0,2 mol), CO32- (0,1k mol), HCO3- (0,15k mol)
BTĐT: 0,225 + 0,2 = 2.0,1k + 0,15k => k = 1,3
BTNT C: nCO2 ban đầu = nBaCO3 + nCO32- + nHCO3- = 0,1 + 0,13 + 0,195 = 0,425 mol
=> V = 9,52 lít

Chọn đáp án C
Nếu Al(OH)3 đã bị hòa tan
⇒
nOH- từ m1 gam rắn ![]()
Mà
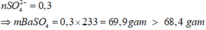
⇒ Al(OH)3 không bị hòa tan và Y còn Al3+ dư ⇒ Y là dung dịch Al2(SO4)3
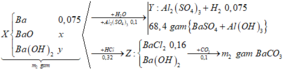
Từ tỉ lệ phản ứng: 3Ba(OH)2 + Al2(SO4)3 ⇒ nBaSO4 : nAl(OH)3 = 3 : 2 ⇒ Đặt là 3a và 2a
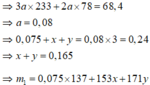
⇒
![]()
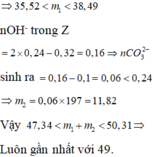

Chọn đáp án A
Với bài toán kim loại tác dụng với muối các bạn cứ quan niệm là kim loại mạnh nhất sẽ đi nuốt anion của thằng yếu nhất trước.
Ta có
![]()
lượng NO3 này sẽ phân bổ dần cho:
Đầu tiên
![]()
![]()
Và Cu + Ag bị cho ra ngoài hết
![]()
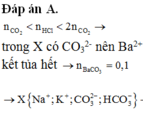
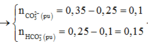
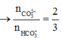


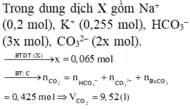
nOH- = 0,02 + ( 0,1.2 ) = 0,22
Đặt tỉ lệ ta có
\(\dfrac{n_{OH^-}}{n_{CO2}}\) = \(\dfrac{0,22}{0,032}\) = 6,875
\(\Rightarrow\) Tạo muối trung hòa
2OH- + CO2 \(\rightarrow\) CO32- + H2O
Từ PTHH ta có tỉ lệ
\(\dfrac{0,22}{2}>\dfrac{0,032}{1}\)
\(\Rightarrow\) OH- dư
\(\Rightarrow\) nCaCO3 = nCO32- = 0,032 (mol)
\(\Rightarrow\) mCaCO3 = 0,032.100 = 3,2 (g)
Để tính khối lượng kết tủa thu được, ta cần tìm số mol các ion Ca2+ và CO32- trong dung dịch, sau đó dựa trên phương trình phản ứng để tính khối lượng kết tủa.
Phương trình phản ứng giữa CO2 và KOH:
CO2 + 2KOH → K2CO3 + H2O
Phương trình phản ứng giữa Ca(OH)2 và CO2:
Ca(OH)2 + CO2 → CaCO3 + H2O
Số mol ion OH- trong dung dịch X:n(OH-) = n(KOH) + 2n(Ca(OH)2) = 0,02 + 2×0,1 = 0,22 mol
Số mol ion HCO3- (tương đương với số mol CO2) trong dung dịch X:n(HCO3-) = n(CO2) = 0,032 mol
Số mol ion CO32- tạo thành sau phản ứng giữa CO2 và ion OH-:n(CO32-) = n(HCO3-) = 0,032 mol
Số mol ion Ca2+ tạo thành sau phản ứng giữa Ca(OH)2 và CO2:n(Ca2+) = n(CO2) = 0,032 mol
Do phản ứng giữa Ca(OH)2 và CO2 xảy ra hoàn toàn nên không có Ca(OH)2 còn dư trong dung dịch.
Khối lượng kết tủa thu được là khối lượng của CaCO3 tạo thành:
m(CaCO3) = n(CaCO3) × M(CaCO3) = (n(Ca2+) + n(CO32-)) × M(CaCO3) = (0,032 + 0,032) mol × 100,09 g/mol = 6,42 g
Vậy khối lượng kết tủa thu được là 6,42 g.