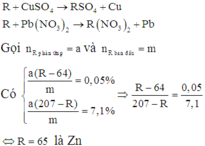hai thanh kim loại giống nhau ( đếu cùng nguyện tố R và cùng khối lượng ), cho thanh thứ nhất vào dung dịch Cu(NO3)2 và thanh thứ 2 vào dung dịch Pb(NO3)2 ,Sau một thời gian khi số mol 2 muối sinh ra bằng nhau lấy hai thanh kim laoij đó ra khỏi dung dịch thấy khối lượng thanh thứ nhất giảm đi 0.2% CÒN THANH THỨ 1 TĂNG 28,45%,xác định nguyên tố R
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


gọi x là số mol của R dã pư,theo bài ra ta có pt
R + Cu(NO3)2 = R(NO3)2 + Cu (1)
x x
R + Pb(NO3)2 = R(NO3)2 + Pb (2)
y y
theo (1) thì kim loại R giảm = kim loại R tan ra - kim loại Cu thoát ra bám vào thanh R
hay Rx - 64x = 0,2% * m <=> (R-64)x = 0,2% * m (I)
theo (2) thì kl R tăng = kim loại Pb thoát ra bám vào thanh R - kl R tan ra trong pư.
hay 207x - Rx = 28,4% * m <=> (207 - R)x = 28,4% * m(II)
chia 2 vế của (II)cho (I) ta được:
(207 - R)/(R-64) = 28,4% * m / 0,2% * m = 28,4/0,2 = 142
<=> 207 - R = 142R - 9088
<=> 143R = 9295
<=> R = 65 đvC (Zn)
vậy R là Zn ( kẽm)
Chúc em học tốt !!

Đáp án C
Tổng khối lượng 2 thanh kim loại sau phản ứng vẫn là 2a gam
=> mthanh 1 tăng = mthanh 2 tăng
Đặt số mol kim loại phản ứng với AgNO3 và Cu(NO3)2 lần lượt là x, y
=> 108 . 2 x - M X . x = M X . y - 64 y ( 1 )
Nồng độ mol của muối kim loại X trong dung dịch Cu(NO3)2 gấp 10 lần trong dung dịch AgNO3.
⇒ y 1 , 5 = 10 . x 0 , 1 ⇒ y = 150 x thay vào (1) được:
108 . 2 x - M X . x = M X . 150 x - 64 . 150 x ⇒ M X = 65 => X là Zn.

Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)

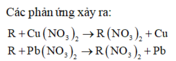
Khối lượng thanh 1 giảm do khối lượng mol của R lớn hơn Cu và khối lượng thanh 2 tăng do khối lượng mol của M nhỏ hơn Pb.
Gọi số mol R đã phản ứng ở 2 trường hợp là a.
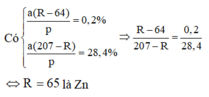
Đáp án C

Giả sử thanh kim loại ban đầu nặng m (g)
Gọi số mol Cu(NO3)2, Pb(NO3)2 pư là a (mol)
TN1:
PTHH: R + Cu(NO3)2 --> R(NO3)2 + Cu
a<-------a------------------>a
=> mgiảm = a.MR - 64a (g)
Và \(m_{giảm}=\dfrac{0,05m}{100}=0,0005m\left(g\right)\)
=> \(a.M_R-64a=0,0005m\) (1)
TN2:
PTHH: R + Pb(NO3)2 --> R(NO3)2 + Pb
a<-------a------------------->a
=> mtăng = 207a - a.MR (g)
Và \(m_{tăng}=\dfrac{7,1.m}{100}=0,071m\left(g\right)\)
=> \(207a-a.M_R=0,071m\) (2)
(1)(2) => \(\dfrac{M_R-64}{207-M_R}=\dfrac{0,0005}{0,071}\)
=> MR = 65 (g/mol)
=> R là Zn

Gọi khối lượng thanh kim loại là: m (g)
M+ Cu(NO3)2→ M(NO3)2+ Cu↓
x___________________________x
M+ Pb(NO3)2→ M(NO3)2+ Pb↓
x__________________________x
Ta có pt:
\(\frac{0,2m}{28,4m}=\frac{x\left(M-64\right)}{x\left(207-M\right)}\)
⇒ M=65
Vậy M là Kẽm: Zn