Hòa tan 100g CuSO4. 5H2O vào 400ml dung dịch HCl 0,6M ta thu được dung dịch A. Chia A làm 2 phần bằng nhau.
a) Cho 5,6g Al vào phần 1, sau một thời gian thu được 1,344 lít khí ở đktc; dung dịch B và chất rắn C. Cho B vào dung dịch NaOH dư rồi lấy kết tủa đem nung ở nhiệt độ cao đến khối lượng không đổi thu được 4g chất rắn. Tính khối lượng chất rắn C.
b) Cho 13,7g Ba vào phần 2, sau khi kết thúc tất cả các phản ứng, lọc lấy kết tủa rửa sạch và nung ở nhiệt độ cao thì thu được bao nhiêu gam chất rắn? Biết rằng khi tác dụng với bazơ CuSO4 chỉ tạo thành Cu(OH)2.





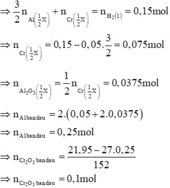


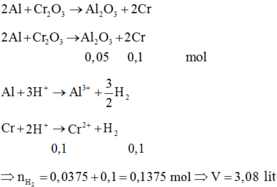
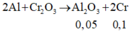
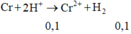

Số mol CuSO4 ban đầu là=100:250 =0,4 mol .Số mol HCl ban đầu =0,36 mol.Vậy mỗi phần có 0,2 mol CuSO4 và 0,12 mol HCl
a)
Số mol Al=0,2 mol.Số mol khí sinh ra là:0,06 mol
Pứ: 2Al + 6HCl ➞ 2AlCl3 + 3H2
0,04 0,12 0,06
Sau pứ này Al còn 0,2-0,04=0,16 mol và phản ứng tiếp với CuSO4 tạo dung dịch B .Dung dịch B tác dụng với xút dư vẫn có kết tủa sauy ra CuSO4 không pứ hết nên còn dư trong dung dịch B .Gọi a là số mol CuSO4 đã phản ứng với Al ta có PT:
2Al + 3CuSO4 ➞ Al2(SO4)3 + 3Cu (3)
2/3a : a (mol)
CuSO4 + 2NaOH ➞ Cu(OH)2 + Na2SO4
(0,2-a) (0,2-a)
Cu(OH)2 ➞ CuO + H2O
(0,2-a) : (0,2-a)
=>0,2-a=0.05=>a=0.15
Vậy lượng chất rắn C=lượng Cu sinh ra ở (3) +lượng Al còn dư =0,15.64+(0.16-2/3*0.15)*27=11.22(g)
Số mol Ba=0,1 mol
Ba+ 2HCl ➞ BaCl2 + H2
0,06 : 0,12 (mol)
Ba còn dư 0,04 mol sẽ phản ứng với tiếp với nước
Ba+ 2H2O ➜ Ba(OH)2 + H2
0,04 : .......... .... 0,04 (mol)
Trong dung dịch khi kết thúc hai pứ trên có số mol Ba2+ = số mol Ba =0,1 mol và số mol OH- =2số mol Ba(OH)2 =0,08 mol
Ba2+ + SO42- ➞ BaSO4 : Cu2+ + 2OH- ➞ Cu(OH)2
0,1 .......(0,2) ...........0,1 ......................0,04 ......0,08 ..........0,04
Chỉ có CuSO4 bị nhiệt phân Cu(OH)2 ➞ CuO + H2O
...................................................0,04........... 0,04
Vậy chất rắn thu đc sau khi nung là=0,1.233+0,04.80=26,5g
bạn tích cho mình được không