Hỗn hợp khí X gồm ( O2 và O3) có tỉ khối so với hiđro là : 21. Tính số mol mỗi khí có trong 8,96 lit hỗn hợp khí X (đktc).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Gọi nO2 =a (mol); nO3 = b(mol)
Có: \(\dfrac{32a+48b}{a+b}=20.2=40\)
=> 32a + 48b = 40a + 40b
=> 8a = 8b => a = b
=> \(\left\{{}\begin{matrix}\%V_{O_2}=\dfrac{a}{a+b}.100\%=\dfrac{a}{a+a}.100\%=50\%\\\%V_{O_3}=100\%-50\%=50\%\end{matrix}\right.\)
b) Gọi nN2 =a (mol); nNO = b(mol)
Có: \(\dfrac{28a+30b}{a+b}=14,75.2=29,5\)
=> 28a + 30b = 29,5a + 29,5b
=> 1,5a = 0,5b
=> 3a = b
=> \(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{a}{a+b}.100\%=\dfrac{a}{a+3a}.100\%=25\%\\\%V_{NO}=100\%-25\%=75\%\end{matrix}\right.\)

Đặt \(n_{O_2}=x;n_{CO_2}=y\)
\(n_X=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Leftrightarrow x+y=0,2\)
Ta có: \(16x+44y=\left(x+y\right).18.2\)
\(\Leftrightarrow2y=5x\)
\(\Leftrightarrow\dfrac{y}{5}=\dfrac{x}{2}\)
Mà x+y=0,2
\(\Rightarrow\dfrac{y}{5}=\dfrac{x}{2}=\dfrac{x+y}{5+2}=\dfrac{0,2}{7}=0,0286\)
\(\Rightarrow y=5.0,0286=0,143\left(mol\right);x=0,2-0,143=0,057\left(mol\right)\)

Ta có: \(n_X=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi: \(\left\{{}\begin{matrix}n_{H_2}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\) ⇒ x + y = 0,4 (mol) (1)
\(d_{X/NO_2}=0,5\Rightarrow M_X=0,5.46=23\left(g/mol\right)\)
⇒ mX = 0,4.23 = 9,2 (g)
⇒ 2x + 44y = 9,2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)

Đáp án B
Nhận thấy :
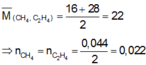
Quy đổi O2 và O3 thành O. Theo bảo toàn electron và bảo toàn khối lượng, ta có :
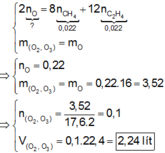

a) Gọi số mol CH4, O2 là a, b (mol)
=> \(\left\{{}\begin{matrix}a+b=\dfrac{8,96}{22,4}=0,4\\M=\dfrac{16a+32b}{a+b}=1.28=28\left(g/mol\right)\end{matrix}\right.\)
=> a = 0,1 (mol); b = 0,3 (mol)
\(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,1}{0,4}.100\%=25\%\\\%V_{O_2}=\dfrac{0,3}{0,4}.100\%=75\%\end{matrix}\right.\)
b)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,3}{2}\) => CH4 hết, O2 dư
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,1--->0,2-------->0,1
=> VCO2 = 0,1.22,4 = 2,24 (l)
=> VO2(dư) = (0,3 - 0,2).22,4 = 2,24 (l)
=> Vkhí = 2,24 + 2,24 = 4,48 (l)

a) \(\overline{M}_A=5,875.2=11,75\left(g/mol\right)\)
b) Gọi số mol N2, H2 là a, b (mol)
\(\overline{M}_A=\dfrac{28a+2b}{a+b}=11,75\left(g/mol\right)\)
=> 16,25a = 9,75b
=> a = 0,6b
\(\left\{{}\begin{matrix}\%n_{N_2}=\dfrac{a}{a+b}.100\%=\dfrac{0,6b}{0,6b+b}.100\%=37,5\%\\\%n_{H_2}=\dfrac{b}{a+b}.100\%=\dfrac{b}{0,6b+b}.100\%=62,5\%\end{matrix}\right.\)
c)
1 mol hỗn hợp A chứa \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{1.37,5}{100}=0,375\left(mol\right)\\n_{H_2}=\dfrac{1.62,5}{100}=0,625\left(mol\right)\end{matrix}\right.\)
\(\overline{M}_B=\dfrac{0,375.28+0,625.2+17x}{1+x}=6,4.2=12,8\left(g/mol\right)\)
=> x = 0,25 (mol)

a) \(M_X=19.2=38\left(g/mol\right)\)
`=>` \(d_{X/kk}=\dfrac{38}{29}=1,310345\)
b) \(m_X=0,4.38=15,2\left(g\right)\)
Gọi \(\left\{{}\begin{matrix}n_{O_2}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}32x+44y=15,2\\x+y=0,4\end{matrix}\right.\Leftrightarrow x=y=0,2\)
\(m_Y=0,1.28+15,2=18\left(g\right)\)
`=>` \(\left\{{}\begin{matrix}\%m_{N_2}=\dfrac{0,1.28}{18}.100\%=15,56\%\\\%m_{O_2}=\dfrac{0,2.32}{18}.100\%=35,56\%\\\%m_{CO_2}=100\%-15,56\%-35,56\%=48,88\%\end{matrix}\right.\)
b) \(M_{hh}=4.10=40\left(g/mol\right)\)
Gọi \(n_{NO_2}=a\left(mol\right)\)
`=>` \(\left\{{}\begin{matrix}m_{hh}=18+46a\left(g\right)\\n_{hh}=0,5+0,1+a=0,6+a\left(mol\right)\end{matrix}\right.\)
`=>` \(M_{hh}=\dfrac{m_{hh}}{n_{hh}}=\dfrac{18+46a}{0,6+a}=40\)
`=> a = 1`
`=> V_{NO_2(đktc)} = 1.22,4 = 22,4 (l)`
Đặt a, b lần lượt số mol O2 và O3 trong hh X. (a,b>0)
=> 22,4a+22,4b=8,96 (1)
Mặt khác:
\(M_{hhX}=21.2=42\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow\dfrac{32a+48b}{a+b}=42\left(2\right)\)
Từ (1), (2) giải hệ được: a=0,15(mol); b=0,25(mol)
=> \(n_{O_2}=0,15\left(mol\right);n_{O_3}=0,25\left(mol\right)\)