Hoà tan 13,6 gam một hỗn hợp gồm Fe và Fe2O3 bằng lượng vừa đủ dung dịch HCl 10%. Sau phản ứng thu được dung dịch X và 2,24 lít khí (đktc). Tính:
a. Thành phần % về khối lượng của hỗn hợp.
b. Khối lượng dung dịch HCl cần dùng.
c. Khối lượng dung dịch X.
d. Nồng độ phần trăm mỗi muối trong dung dịch X.

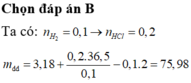
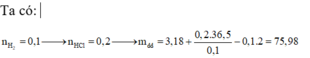
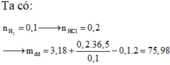
a,\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + 2HCl → FeCl2 + H2
Mol: 0,1 0,2 0,1 0,1
PTHH: Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Mol: 0,05 0,3 0,1
\(m_{Fe}=0,1.56=5,6\left(g\right);m_{Fe_2O_3}=13,6-5,6=8\left(g\right)\)
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
b,\(m_{HCl}=\left(0,2+0,3\right).98=49\left(g\right)\)
\(m_{ddHCl}=\dfrac{49.100}{10}=490\left(g\right)\)
c,\(m_{ddX}=13,6+490-0,1.2=503,4\left(g\right)\)
d,\(C\%_{FeCl_2}=\dfrac{0,1.127.100\%}{503,4}=2,52\%\)
\(C\%_{FeCl_3}=\dfrac{0,05.162,5.100\%}{503,4}=1,614\%\)
mik nhầm C%FeCl3
Sửa lại: \(C\%_{FeCl_3}=\dfrac{0,1.162,5.100\%}{503,4}=3,228\%\)