Cho 13g kẽm tác dụng với HCl theo sơ đồ phản ứng
Zn + HCl ----> ZnCl2 + H2
a, Lập PTHH
b, Tính khối lượng HCl đã tham gia phản ứng
c, Tính thể tích khí H2 (ĐKTC) đã sinh ra sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
___0,3____0,6_____0,3____0,3 (mol)
a, \(m_{Zn}=0,3.65=19,5\left(g\right)\)
b, \(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
c, \(m_{ZnCl_2}=0,3.136=40,8\left(g\right)\)
Bạn tham khảo nhé!

$PTHH:Zn+2HCl\to ZnCl_2+H_2\uparrow$
$n_{Zn}=\dfrac{13}{65}=0,2(mol)$
Theo PT: $n_{ZnCl_2}=n_{H_2}=0,2(mol);n_{HCl}=0,4(mol)$
$a)m_{axit}=m_{HCl}=n.M=0,4.36,5=14,6(g)$
$b)m_{ZnCl_2}=n.M=0,2.136=27,2(g)$
$c)V_{H_2(đktc)}=n.22,4=0,2.22,4=4,48(lít)$
Số mol kẽm là :
\(n=\dfrac{m}{M}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH : Zn + 2HCL -> ZnCl2 + H2
1 2 1 1
0,2 mol -> 0,4 mol 0,2 mol 0,2 mol
a, Khối lượng HCL là :
\(m=n.M=0,4.35,5=14,2\left(g\right)\)
b, Khối lượng ZnCL2 là :
\(m=n.M=0,1.136=13,6\left(g\right)\)
c, Thể tích H2 là : V = n . 22,4 = \(0,1.22,4=2,24\left(l\right)\)

a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Ta có: \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b, Theo PT: \(n_{HCl}=2n_{Zn}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)

a) Số mol kẽm tham gia phản ứng : \(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{16,25}{65}=0,25\left(mol\right)\).
PTHH : \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Mol : 1 : 2 : 1 : 1
Mol : 0,25 → 0,5 → 0,25 → 0,5
Suy ra, số mol dung dịch Axit Clohidric \(HCl\) tham gia phản ứng là \(n_{HCl}=0,5\left(mol\right)\).
Khối lượng dung dịch đã dùng : \(m_{HCl}=n_{HCl}.M_{HCl}=\left(0,5\right).\left(36,5\right)=18,25\left(g\right)\).
b) Từ câu a, suy ra số mol khí Hidro sinh ra là \(n_{H_2}=0,25\left(mol\right)\).
Thể tích khí Hydro sinh ra là : \(V_{H_2}=n_{H_2}.22,4=\left(0,25\right).\left(22,4\right)=5,6\left(l\right)\)

a) pư thuộc loại phản ứng thế
b) \(n_{Zn}=\dfrac{1,3}{65}=0,02\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,02 0,04 0,02 0,02
\(m_{ZnCl_2}=136.0,02=2,72\left(g\right)\\
V_{H_2}=0,02.22,4=0,448\left(l\right)\\
C_{M\left(HCl\right)}=\dfrac{0,04}{0,4}=0,1M\)
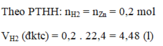
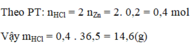

nZn = \(\dfrac{13}{65}\)= 0,2mol
Zn + 2HCl -> ZnCl2 + H2
0,2->0,4 ->0,2
=>mHCl = 0,4 . 36,5 = 14,6 g
=>VH2 = 0,2 . 22,4 = 4,48 (l)
a) ta có nZn= \(\dfrac{13}{65}\)= 0,2( mol)
PTPU
Zn+ 2HCl\(\rightarrow\) ZnCl2+ H2
0,2...0,4.....................0,2..
b) mHCl= 0,4. 36,5=14,6( g)
c) VH2= 0,2. 22,4= 4,48( lít)