a là dung dịch NaOH 0,2M; b lad dung dịch NaOh 0,5M
a) Cần pha bao nhiêu ml a với 2,5 l b để được dung dịch c có nồng độ 0,3M
b) Cho 0,5 l b phản ứng với 200 g dung dịch HCl 36,5 %. Tính khối lượng các chất tan trong phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Dung dịch C có pH =7 ⇒ nH+ = nOH- ⇒ 0,1.0,1.2 + 0,2.0,1 = 0,2V + 0,3V
⇒ V =0,08l = 80 ml
Đáp án D.

Đáp án : D
Trong A :
n H + = 2 n H 2 S O 4 + n H N O 3 + n H C l = 0,21 mol
Trong B :
n O H - = nNaOH + nKOH = 0,49V mol
Để C có pH = 2 (axit) => H+ dư
=> nH+(C) = 10-pH .(0,3 + V) = 0,21 – 0,49V
=> V = 0,414 lit

Đáp án A
nH+= nHCl+ 2nH2SO4+ 3nH3PO4= 0,1.0,3+ 2.0,2.0,1+ 3.0,1.0,1=0,1 mol
nOH-= (V.0,1+2.0,2.V)/1000 mol
H+ + OH-→ H2O
Theo PT: nH+= nOH- nên 0,1=(V.0,1+2.0,2.V)/1000 suy ra V= 200 ml

Đáp án A
Hướng dẫn
VX = V; nC6H5OH = 0,2 x 0,2 = 0,04 mol.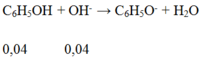
nOH- = 0,2V + 0,3V = 0,04
→ V = 0,08 lít = 80 ml

Đáp án A
VX = V; nC6H5OH = 0,2 x 0,2 = 0,04 mol.
C6H5OH + OH- → C6H5O- + H2O
0,04----------0,04
nOH- = 0,2V + 0,3V = 0,04
→ V = 0,08 lít = 80 ml

a, \(n_{NaOH}=0,15.0,2=0,03\left(mol\right)=n_{Na^+}=n_{OH^-}\)
\(n_{KOH}=0,15.0,2=0,03\left(mol\right)=n_{K^+}=n_{OH^-}\)
⇒ ΣnOH- = 0,03 + 0,03 = 0,06 (mol)
\(n_{HCl}=0,25.0,4=0,1\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(H^++OH^-\rightarrow H_2O\)
0,06____0,06 (mol) ⇒ nH+ dư = 0,1 - 0,06 = 0,04 (mol)
\(\left[Na^+\right]=\left[K^+\right]=\dfrac{0,03}{0,15+0,25}=0,075\left(M\right)\)
\(\left[H^+\right]=\dfrac{0,04}{0,15+0,25}=0,1\left(M\right)\)
\(\left[Cl^-\right]=\dfrac{0,1}{0,15+0,25}=0,25\left(M\right)\)
b, pH = -log[H+] = 1

a, \(n_{HCl}=0,1.0,2=0,02\left(mol\right)=n_{H^+}=n_{Cl^-}\)
\(n_{H_2SO_4}=0,1.0,2=0,02\left(mol\right)=n_{SO_4^{2-}}\) \(\Rightarrow n_{H^+}=2n_{H_2SO_4}=0,04\left(mol\right)\)
\(n_{NaOH}=0,3.0,4=0,12\left(mol\right)=n_{Na^+}=n_{OH^-}\)
\(\Rightarrow\sum n_{H^+}=0,02+0,04=0,06\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
0,06__0,06 (mol)
⇒ nOH- dư = 0,12 - 0,06 = 0,06 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\left[Cl^-\right]=\dfrac{0,02}{0,1+0,3}=0,05\left(M\right)\\\left[SO_4^{2-}\right]=\dfrac{0,02}{0,1+0,3}=0,05\left(M\right)\\\left[Na^+\right]=\dfrac{0,12}{0,1+0,3}=0,3\left(M\right)\\\left[OH^-\right]=\dfrac{0,06}{0,1+0,3}=0,15\left(M\right)\end{matrix}\right.\)
b, pH = 14 - (-log[OH-]) ≃ 13,176
a) Gọi Va là x, ta có
\(\dfrac{0,2x+1,25}{x+2,5}\)=0,3⇌ x=0,5 l=500ml
b) Ta có PTHH: NaOH+ HCl→H2O+ NaCl
nHCl= (200:100.36,5):36.5=2 mol
n NaOH=0,5.0,5=0,25 mol
⇒Sau pư HCl dư: 36,5.(2-0,25)=63,875g
mNaCl=(23+35,5).0.25=14,525g
a) Gọi Va là x, ta có
0,2x+1,25x+2,50,2x+1,25x+2,5=0,3⇌ x=0,5 l=500ml
b) Ta có PTHH: NaOH+ HCl→H2O+ NaCl
nHCl= (200:100.36,5):36.5=2 mol
n NaOH=0,5.0,5=0,25 mol
⇒Sau pư HCl dư: 36,5.(2-0,25)=63,875g
mNaCl=(23+