cho 20,2 gam hỗn hợp bột Zn và Feo vào lượng dư dung dịch CuSO4.Sau khi phản ứng kết thúc các phản ứng, lọc bỏ phần dung dịch thu được m gam bột rắn. cho bột rắn thu được tác dụng với HCl thu được 12,8 gam chất rắn đỏ kết tủa. tính % các chất trong hỗn hợp ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B.
Gọi số mol của Zn và Fe lần lượt là x và y mol
PTHH:
Zn + CuSO4 à ZnSO4 + Cu
x à x
Fe + CuSO4 à FeSO4 + Cu
y à y
Theo bài ta có: mrắn bđ = mrắn sau ó 65x + 56y = 64x + 64y ó x = 8y.
Coi số mol của Fe là 1 mol thì số mol của Zn là 8 mol.
Thành phần phần trăm theo khối lượng của Zn trong hỗn hợp bột ban đầu là:
![]()

Đáp án A
Ta có dãy điện hóa: ![]()
=>Zn phản ứng với C u 2 + trước
![]() khối lượng rắn giảm
khối lượng rắn giảm
![]() khối lượng rắn tăng
khối lượng rắn tăng
Do cuối cùng m rắn = m(g) =m hỗn hợp ban đầu =>tăng và giảm phải cân bằng với nhau.
Đặt nZn = x; nFe = y => m giảm = (65 - 64)x = x(g); m tăng = (64 - 65)y = 8y
m tăng = m giảm =>x = 8y =>%mZn = 65x/(65x - 56y)x100% = 90,27%

Đáp án A
► Đặt nZn = x; nFe = y. Do Cu2+ dư nên ta có:
– Zn + Cu2+ → Zn2+ + Cu ||⇒ tăng (65 – 64)x = x (g).
– Fe + Cu2+ → Fe2+ + Cu ||⇒ giảm (64 – 56)y = 8y (g).
Do mrắn = mkim loại ban đầu = m(g) ⇒ x = 8y.
||⇒ %mZn = 65 × 8y ÷ (65 × 8y + 56y) × 100% = 90,27%

Đáp án A
Ta có dãy điện hóa: ![]()
=>Zn phản ứng với C u 2 + trước
![]()
=> Khối lượng rắn giảm
![]() => Khối lượng rắn tăng
=> Khối lượng rắn tăng
Do cuối cùng m rắn = m(g) =m hỗn hợp ban đầu =>tăng và giảm phải cân bằng với nhau.
Đặt n Z n = x ; n F e = y => m giảm = (65 - 64)x = x(g); m tăng = (64 - 56)y = 8y
m tăng = m giảm => x = 8y => %mZn = 65x : (65x - 56y).100% = 90,27%



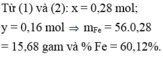

Chất rắn đỏ kết tủa cuối cùng là Cu: 0,2 -> nCuSO4 = 0,2
Ta có: nZn = nCuSO4 = 0,2
=> Phần trăm khối lượng mỗi chất