đốt cháy hoàn toàn 7,6 gam hỗn hợp gồm Cu, Mg tronh õi thì thu dc một hỗn hợp oxit có 20% MgO và 80% CuO vè khối lượng. Hòa tan hỗn hợp vào dung dịch HCl 0,5M
a/ xác định số gam mỗi kim loạii trong hỗn hợp đầu.
b/ tính thể tích dung dịch HCl phải dùng để hòa tan hết lượng oxit kim lọai sau khi đốt cháy.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a/ Gọi x và y là số mol của Cu và Mg ban đầu.
Ta có: 64x + 24y = 7.6 g
<=> 8x + 3y = 0.95 (1)
2Cu + O2 ---------------> 2CuO
x ------------------------------ x mol
2Mg + O2 ---------------> 2MgO
y ------------------------------ y mol
Từ 2 ptpứ ta có KL hỗn hợp sau pứ là: m = 80x + 40y
Vì KL MgO chiếm 20% KL hỗn hợp nên:
\(\dfrac{40y}{80x+40y}\) = 20% = 0.2
<=> 40y = 0.2(80x + 40y)
<=> 40y = 16x + 8y
<=> 32y = 16x
<=> x = 2y. Thế vào (1) ta có:
<=>8.2y + 3y = 0.95
<=> 19y =0.95
<=> y = 0.05 mol.
===> x = 2.0.05 = 0.1 mol.
Vậy khối lượng Mg: m = 0.05.24 = 1.2 g
mCu: m = 7.6 - 1.2 = 6.4 g.
b/
2HCl `+ `CuO -------> CuCl2 + H2O
0.2 <--- 0.1 mol
2HCl ` + `MgO ------> MgCl2 + H2O
0.2 <----- 0.1 mol
Từ 2 pt trên ta tính lượng axit HCl nguyên chất cần dùng: n = 0.2 + 0.2 = 0.4 mol.
=>VHCl=\(\dfrac{0,4}{0,5}\)=0,8l=800ml

a) Gọi số mol Cu, Mg là a, b (mol)
=> 64a + 24b = 7,6 (1)
PTHH: 2Cu + O2 --to--> 2CuO
a---------------->a
2Mg + O2 --to--> 2MgO
b------------------>b
=> \(\%MgO=\dfrac{40b}{80a+40b}.100\%=20\%\)
=> a = 2b (2)
(1)(2) => a = 0,1; b = 0,05
=> \(\left\{{}\begin{matrix}m_{Cu}=0,1.64=6,4\left(g\right)\\m_{Mg}=0,05.24=1,2\left(g\right)\end{matrix}\right.\)
b)
PTHH: CuO + H2SO4 --> CuSO4 + H2O
0,1--->0,1
MgO + H2SO4 --> MgSO4 + H2O
0,05--->0,05
=> \(V_{ddH_2SO_4}=\dfrac{0,1+0,05}{0,5}=0,3\left(l\right)\)
Ủa anh ra khác em luôn...để anh xem lại

Bài này ta hiểu là pứ đã hết CuSO4, và Cu tạo thành đã bám vào đinh, nên khối lượng chiếc đinh mới tăng, và Fe pứ đã tan vào dung dịch.
Gọi x là số mol fe đã pứ. x > 0
`
Fe + CuSO4 =-------------------> FeSO4 + Cu
x -------- x ----------------------------------------... x mol
`
Vậy KL tăng sau pứ là do hiệu giữa KL Cu bám vào và KL Fe đã tan ra. m = 0.8 = 64x - 56x
<=> x = 0.1 mol
KL Cu m= 64*0.1 = 6.4 g
KL Fe pứ: m = 56*0.1 5.6 g
Nồng độ mol dung dịch CuSO4 ban đầu: C = 0.1/0.2 = 0.5 M

mO = 5,96 - 4,04 = 1,92 (g)
=> \(n_O=\dfrac{1,92}{16}=0,12\left(mol\right)\)
=> \(n_{H_2O}=0,12\left(mol\right)\)
=> \(n_{HCl}=0,24\left(mol\right)\)
=> \(V_{ddHCl}=\dfrac{0,24}{2}=0,12\left(l\right)\)

Ta có sơ đồ phản ứng:
m(gam) (Mg, Fe) + --O2→ (m+4,16) gam B + --HCl→ D (Mg2+ x mol; Fe2+ y mol; Fe3+ z mol); Cl-)
D + --AgNO3→ (11m – 12,58) gam (Ag + AgCl)
Ta có m(O) = 4,16 gam → n(O) = 0,26 mol → n(Cl- trong D) = 0,52 mol
→ n(AgCl) = 0,52 mol
Ta có hệ phương trình
(1): 24x + 56(y+z) = m
(2) ĐLBT điện tích: 2x+2y+ 3z = 0,52
(3) m + 0,52*35,5 = 4m-6,5
→ m = 8,32 gam → n(Ag) = 0,04 = y → x = 0,16; z = 0,04
Mặt khác trong 4,5m gam A có: Mg = 0,72 mol và Fe 0,36 mol
Dung dịch muối: Mg2+: 0,72 mol; Fe3+: 0,36mol; NH4+: t mol; NO3-: q mol
hợp khí F gồm N2 (0,04 mol) và N2O (0,04 mol)
Áp dụng ĐLBT mol e: → t = 0,225 mol
Áp dụng ĐLBT điện tích → q = 2,745 mol → m 211,68 gam → Đáp án C

Đáp án C
Ta có sơ đồ phản ứng:
m(gam) (Mg, Fe) + --O2→ (m+4,16) gam B + --HCl→ D (Mg2+ x mol; Fe2+ y mol; Fe3+ z mol); Cl-)
D + --AgNO3→ (11m – 12,58) gam (Ag + AgCl)
Ta có m(O) = 4,16 gam → n(O) = 0,26 mol → n(Cl- trong D) = 0,52 mol
→ n(AgCl) = 0,52 mol
Ta có hệ phương trình
(1): 24x + 56(y+z) = m
(2) ĐLBT điện tích: 2x+2y+ 3z = 0,52
(3) m + 0,52*35,5 = 4m-6,5
→ m = 8,32 gam → n(Ag) = 0,04 = y → x = 0,16; z = 0,04
Mặt khác trong 4,5m gam A có: Mg = 0,72 mol và Fe 0,36 mol
Dung dịch muối: Mg2+: 0,72 mol; Fe3+: 0,36mol; NH4+: t mol; NO3-: q mol
hợp khí F gồm N2 (0,04 mol) và N2O (0,04 mol)
Áp dụng ĐLBT mol e: → t = 0,225 mol
Áp dụng ĐLBT điện tích → q = 2,745 mol → m 211,68 gam

Đáp án C
Ta có sơ đồ phản ứng:
m(gam) (Mg, Fe) + --O2→ (m+4,16) gam B + --HCl→ D (Mg2+ x mol; Fe2+ y mol; Fe3+ z mol); Cl-)
D + --AgNO3→ (11m – 12,58) gam (Ag + AgCl)
Ta có m(O) = 4,16 gam → n(O) = 0,26 mol → n(Cl- trong D) = 0,52 mol
→ n(AgCl) = 0,52 mol
Ta có hệ phương trình
(1): 24x + 56(y+z) = m
(2) ĐLBT điện tích: 2x+2y+ 3z = 0,52
(3) m + 0,52*35,5 = 4m-6,5
→ m = 8,32 gam → n(Ag) = 0,04 = y → x = 0,16; z = 0,04
Mặt khác trong 4,5m gam A có: Mg = 0,72 mol và Fe 0,36 mol
Dung dịch muối: Mg2+: 0,72 mol; Fe3+: 0,36mol; NH4+: t mol; NO3-: q mol
hợp khí F gồm N2 (0,04 mol) và N2O (0,04 mol)
Áp dụng ĐLBT mol e: → t = 0,225 mol
Áp dụng ĐLBT điện tích → q = 2,745 mol → m 211,68 gam
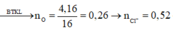
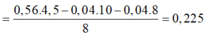
a/ Gọi x và y là số mol của Cu và Mg ban đầu.
Ta có: 64x + 24y = 7.6 g
<=> 8x + 3y = 0.95 (1)
2Cu + O2 ---------------> 2CuO
x ------------------------------ x mol
`
2Mg + O2 ---------------> 2MgO
y ------------------------------ y mol
`
Từ 2 ptpứ ta có KL hỗn hợp sau pứ là: m = 80*x + 40*y
Vì KL MgO chiếm 20% KL hỗn hợp nên:
40y/(80*x + 40*y) = 20% = 0.2
<=> 40y = 0.2(80*x + 40*y)
<=> 40y = 16x + 8y
<=> 32y = 16x
<=> x = 2y. Thế vào (1) ta có:
`
<=>8*2y + 3y = 0.95
<=> 19y =0.95
<=> y = 0.05 mol.
===> x = 2*0.05 = 0.1 mol.
Vậy khối lượng Mg: m = 0.05*24 = 1.2 g
KL Cu: m = 7.6 - 1.2 = 6.4 g.
phần b mình làm ko ra