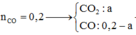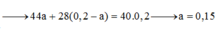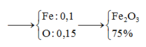2.Dẫn 2,8 l CO đktc đi qua bình đựng 4,5 g một oxit sắt thì thu đc m g sắt và hỗn hợp khí A có tỉ khối đối với H2 là 18.Hãy tính m sắt và xđ CTHH của oxit sắt
[ phản ứng xảy ra hoàn toàn và theo sơ đồ sau FexOy+CO ==>Fe+CO2]
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Cho hỏi chỗ sơ đồ đường chéo 4 và 12 là như nào đấy ạ .___.
Còn cả chỗ suy ra 42x-28y=0

Đặt CTHH oxit sắt: \(Fe_xO_y\)
\(Fe_xO_y+yCO\rightarrow\left(t^o\right)xFe+yCO_2\)
hh khí A gồm: khí CO2 và có thể có CO (dư)
\(d_{\dfrac{A}{H_2}}=22\) \(\Rightarrow M_A=22.2=44\) \((g/mol)\)
\(\Leftrightarrow\dfrac{44n_{CO_2}+28n_{CO\left(dư\right)}}{n_{CO_2}+n_{CO\left(dư\right)}}=44\)
\(\Leftrightarrow16n_{CO\left(dư\right)}=0\)
\(\Leftrightarrow n_{CO\left(dư\right)}=0\left(mol\right)\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,15 0,15 ( mol )
\(n_{CaCO_3}=\dfrac{15}{100}=0,15\left(mol\right)\)
Bảo toàn O: \(n_{O\left(Fe_xO_y\right)}=n_{CO_2}=0,15\left(mol\right)\)
\(\Rightarrow n_{Fe\left(Fe_xO_y\right)}=\dfrac{8-0,15.16}{56}=0,1\left(mol\right)\)
\(\dfrac{x}{y}=\dfrac{0,1}{0,15}=\dfrac{2}{3}\) \(\Rightarrow\) CTHH: \(Fe_2O_3\)
\(V_{CO}=V_{CO_2}=0,15.22,4=3,36\left(l\right)\)

PTHH: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Đặt \(\left\{{}\begin{matrix}n_{Fe\left(oxit\right)}=a\left(mol\right)=n_{H_2}\\n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có: \(m_{tăng}=m_{Fe}-m_{H_2}\) \(\Rightarrow56a-2a=3,24\) \(\Rightarrow a=n_{Fe}=0,06\left(mol\right)\)
Hỗn hợp D gồm \(\left\{{}\begin{matrix}n_{CO_2\left(dư\right)}=c\left(mol\right)\\n_{H_2O}=n_{O\left(oxit\right)}=b\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}c+b=0,1\\18b+2c=7,4\cdot2\cdot\left(b+c\right)\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}b=0,08\\c=0,02\end{matrix}\right.\)
\(\Rightarrow x:y=a:b=0,06:0,08=3:4\)
\(\Rightarrow\) Công thức cần tìm là Fe3O4