đốt cháy 1kg than trong khí o2, biết than có 10% tạp chất không cháy tính:
- thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên
-khối lượng co2(đktc) sinh ra trong phản ứng trên
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đổi 1kg = 1000g
mC = 1000 . (100% - 10%) = 900 (g)
nC = 900/12 = 75 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 75 ---> 75
VO2 = 75 . 22,4 . 5 = 8400 (l)

Lượng than nguyên chất:
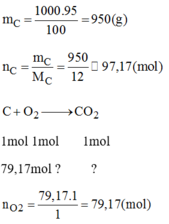
V O 2 = n O 2 .22,4 = 79,17.22,4 = 1773,4(l)

a/ trong 1 kg than có 5% tạp chất ko cháy => 95% khí cacbon cháy dc ( ko bik khoảng nì đúng ko >: mik ko chắc về cách trình bày chặng này bạn thông cảm )
=> Khối lượng cacbon có trong 1kg than:
\(1.95\%=0,95\)(kg) \(=950g\)
CTHH :\(C+O_2\rightarrow CO_2\)
1 : 1 : 1
475 : 475 : 475
\(n_c=\frac{m_c}{M_c}=\frac{950}{2}=475\left(mol\right)\)
\(n_{O_2}=\frac{475.1}{1}=475\left(mol\right)\)
\(V_{O_2}=n_{O_2}.22,4=475.22,4=10640\left(l\right)\)
B/ \(n_{CO_2}=\frac{475.1}{1}=475\left(mol\right)\)
\(V_{CO_2}=n_{CO_2}.22,4=475.22,4=10640\left(l\right)\)

mC = 1000.95% = 950 (g)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Ta có: \(n_C=\dfrac{950}{12}=\dfrac{475}{6}\left(mol\right)\)
Theo PT: \(n_{O_2}=n_{CO_2}=n_C=\dfrac{475}{6}\left(mol\right)\)
a+b, \(V_{O_2}=V_{CO_2}=\dfrac{475}{6}.22,4\approx1773,33\left(l\right)\)

Lượng than nguyên chất:
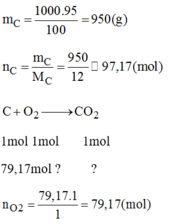
n C O 2 = n O 2 = 79,17(mol) → V C O 2 = V O 2 = 1773,4(l)

\(n_C=\dfrac{7,5.96\%}{12}=0,6\left(mol\right)\\ C+O_2-^{t^o}\rightarrow CO_2\\ n_{O_2}=n_C=0,6\left(mol\right)\\ \Rightarrow V_{O_2}=0,6.22,4=13,44\left(l\right)\)

Đổi 2,5kg = 2500g
mC = 2500 . (100% - 16%) = 2100 (g)
nC = 2100/12 = 175 (mol)
PTHH: C + O2 -> (t°) CO2
Mol: 175 ---> 175 ---> 175
VO2 = 175 . 22,4 = 3920 (l)
mCO2 = 44 . 175 = 7700 (g)
\(m_C=\dfrac{2,5.\left(100-16\right)}{100}=2,1kg\)
\(m_C=2,1kg=2100g\)
\(n_C=\dfrac{m_C}{M_C}=\dfrac{2100}{12}=175mol\)
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
175 175 175 ( mol )
\(V_{O_2}=n_{O_2}.22,4=175.22,4=3920l\)
\(m_{CO_2}=n_{CO_2}.M_{CO_2}=175.44=7700g\)
Cnguyên chất = (100%-10%).1000 = 900 (g)
\(n_C=\dfrac{900}{12}=75\left(mol\right)\)
PTHH: C + O2 ---to→ CO2
Mol: 75 75
\(V_{O_2}=75.22,4=1680\left(l\right)\)
\(m_{CO_2}=75.44=3300\left(g\right)\)