Bài 1
a, Từ hóa chất cho sẵn sau : Fe , H2O với các thiết bị cần thiết đầy đủ Hãy lm thế nào để có thể thực hiện được sự biến đổi sau Fe->Fe3O4->Fe
b,bằng phương pháp hóa học hãy phân biệt các gói bột : vôi sống magie oxit, điphotpho penta oxit, natriclorua, natri oxit
Bài 2 Nung hoàn toàn 15,15g chất rắn A thu được chất rắn B và 1,68 l khí oxi(đktc).Trong hợp chất B có thành phần % khối lượng các nguyên tố 37,65% oxi, 16,47% nitở còn lại là kali. Xác định CTHH của B và A biết rằng CT đơn giản của A, B

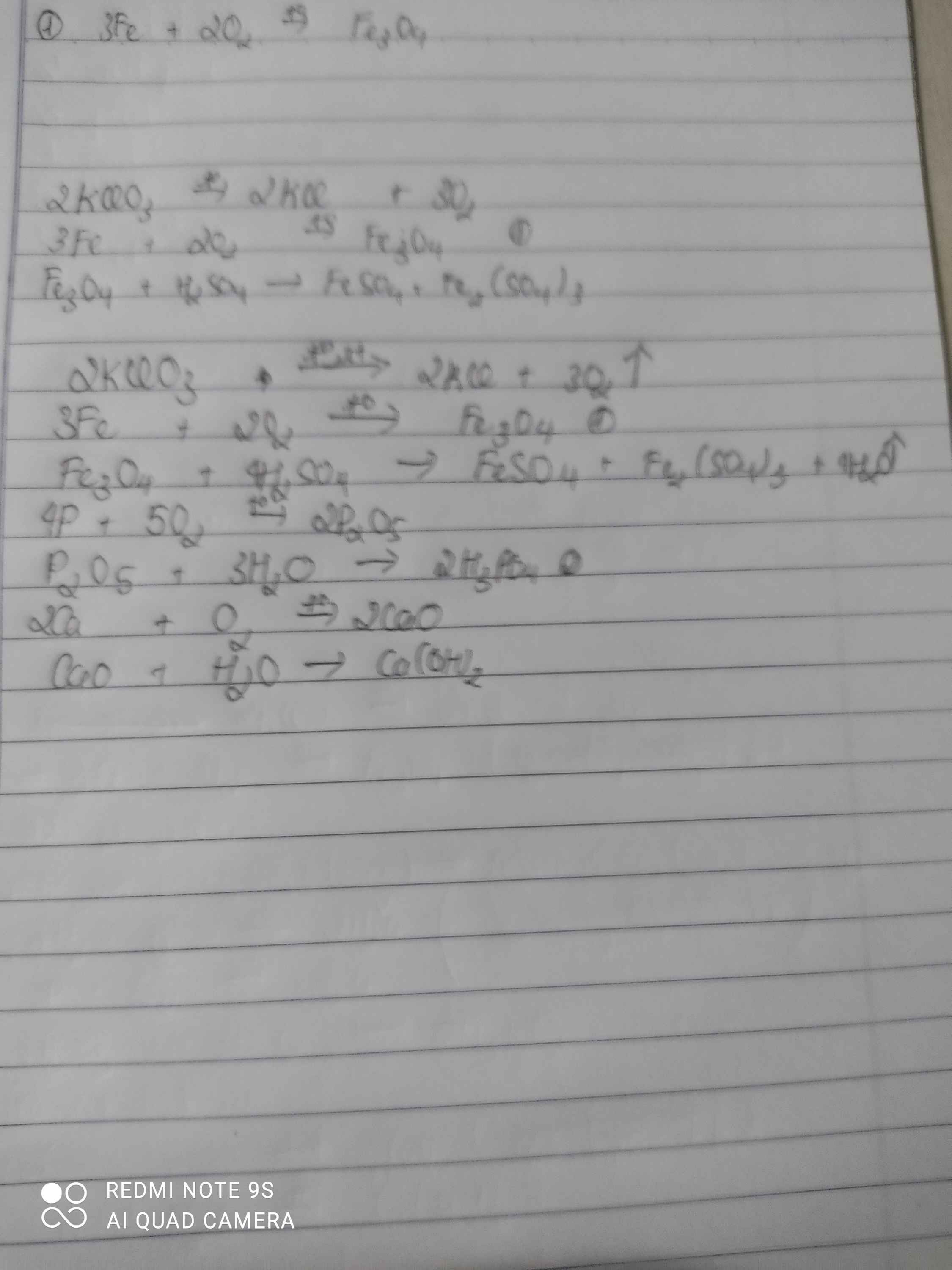
Bài 1:
a) - Điện phân nước:
2H2O --đp--> 2H2 + O2
Pt: 3Fe + 2O2 --to--> Fe3O4
......Fe3O4 + 4H2 --to--> 3Fe + 4H2O
b) - Trích mỗi chất một ít làm mẫu thử
- Cho nước vào các mẫu thử
+ Các mẫu tan gồm: CaO, P2O5, NaCl, Na2O
..............CaO + H2O --> Ca(OH)2
...............P2O5 + 3H2O --> 2H3PO4
...............Na2O + H2O --> 2NaOH
+ Mẫu không tan: MgO
- Nhúng quỳ tím vào các dd:
+ Mẫu làm quỳ tím chuyển sang màu xanh: Ca(OH)2, NaOH chất ban đầu là CaO, Na2O
+ Mẫu làm quỳ tím chuyển sang màu đỏ: H3PO4 chất ban đầu là P2O5
+ Mẫu không làm đổi màu quỳ tím là NaCl
- Dẫn CO2 từ từ vào 2 dd làm quỳ tím chuyển sang màu xanh
+ Mẫu xuất hiện kết tủa là Ca(OH)2 chất ban đầu là CaO
............Ca(OH)2 + CO2 --> CaCO3 + H2O
+ Mẫu còn lại là NaOH chất ban đầu là Na2O
............2NaOH + CO2 --> Na2CO3 + H2O
Bài 2:
A---t*--->B+O2
nO2=1,68/22,4=0,075(mol)
=>mO2=0,075.32=2,4(g)
Áp dụng định luật bảo toàn khối lượng:
mA=mB+mO2
=>mB=mA-mO2=15,15-2,4=12,75(g)
=>mO=12,75.37,65%=4,8(g)=>nO=4,8/16=0,3(mol)
mN=12,75.16,47%=2,1(g)=>nN=2,1/14=0,15(mol)
mK=12,75-4,8-2,1=5,85(g)=>nK=5,85/39=0,15(mol)
Gọi CTHH của B là :KaNbOc
Ta có: a:b:c=nK:nN:nO=0,15:0,15:0,3=1:1:2
===>CTĐG: KNO2
Gọi CTHH của A là: KxNyOz
Định luật bảo toàn nguyên tố:
mO2=4,8+2,4=7,2(g)
=>nO2=0,45(mol)
nN=0,15(mol)
nK=0,15(mol)
Ta có: x:y:z=nK:nN:nO=0,15:0,15:0,45=1:1:3
===>CTHH của A: KNO3