đem phân hủy hoàn toàn gồm 8,77 gam hỗn hợp gồm kclo3 ,kmno4 thu được 1,12l khí o2 ở đktc
a,viết các pthh xảy ra
b,tinhs thành phần phần trăm theo kl mỗi chất ban đầu
c,,tinhs thành phần phần trăm theo kl mỗi chất rắn trong hỗn hợp chất rắn ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1)
Gọi số mol KMnO4, KClO3 là a, b (mol)
=> 158a + 122,5b = 308,2 (1)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------------------------->0,5a
2KClO3 --to--> 2KCl + 3O2
b------------------>1,5b
=> mO2 = (0,5a + 1,5b).32 = 16a + 48b (g)
mD = 308,2 - 16a - 48b(g)
\(m_{Mn}=\dfrac{\left(308,2-16a-48b\right).10,69}{100}=32,94658-1,7104a-5,1312b\left(g\right)\)
=> \(n_{Mn}=\dfrac{32,94658-1,7104a-5,1312b}{55}=0,6-\dfrac{1069}{34375}a-\dfrac{3207}{34375}\left(mol\right)\)
Mà \(n_{Mn}=n_{KMnO_4}=a\left(mol\right)\)
=> \(\dfrac{35444}{34375}a+\dfrac{3207}{34375}b=0,6\) (2)
(1)(2) => a = 0,4 (mol); b = 2 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KMnO_4}=\dfrac{0,4.158}{308,2}.100\%=20,506\%\\\%m_{KClO_3}=\dfrac{2.122,5}{308,2}.100\%=79,494\%\end{matrix}\right.\)
2)
Giả sử nung 100 (g) đá vôi
=> \(m_{CaCO_3\left(bđ\right)}=\dfrac{80.100}{100}=80\left(g\right)\)
\(m_{rắn.sau.pư}=\dfrac{100.73,6}{100}=73,6\left(g\right)\)
=> mCO2 = 100 - 73,6 = 26,4 (g)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\)
PTHH: CaCO3 --to--> CaO + CO2
0,6<----------------0,6
=> mCaCO3(pư) = 0,6.100 = 60 (g)
\(H\%=\dfrac{60}{80}.100\%=75\%\)

a)
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\) (1)
\(2KClO_3\xrightarrow[]{t^o}2KCl+3O_2\) (2)
\(n_{KCl}=\dfrac{0,894}{74,5}=0,012\left(mol\right);m_B=\dfrac{0,894}{8,132\%}=11\left(g\right)\)
Gọi \(n_{O_2\left(sinh.ra\right)}=a\left(mol\right)\Rightarrow n_{kk}=3a\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{N_2}=3a.80\%=2,4a\left(mol\right)\\n_{O_2}=a+\left(3a-2,4a\right)=1,6a\left(mol\right)\end{matrix}\right.\)
\(n_C=\dfrac{0,528}{12}=0,044\left(mol\right)\)
\(C+O_2\xrightarrow[]{t^o}CO_2\) (3)
Vì hỗn hợp D gồm 3 khí và O2 chiếm 17,083%
\(\Rightarrow D:CO_2,O_{2\left(d\text{ư}\right)},N_2\)
BTNT C: \(n_{CO_2}=n_C=0,044\left(mol\right)\)
BTNT O: \(n_{O_2\left(d\text{ư}\right)}=n_{O_2\left(b\text{đ}\right)}-n_{CO_2}=1,6a-0,044\left(mol\right)\)
\(\Rightarrow\%V_{O_2}=\%n_{O_2}=\dfrac{1,6a-0,044}{1,6a-0,044+0,044+2,4a}.100\%=17,083\%\)
\(\Leftrightarrow a=0,048\left(mol\right)\left(TM\right)\)
ĐLBTKL: \(m_A=m_B+m_{O_2}=11+0,048.32=12,536\left(g\right)\)
Theo PT (2): \(n_{KClO_3}=n_{KCl}=0,012\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{0,012.122,5}{12,536}.100\%=11,63\%\\\%m_{KMnO_4}=100\%-11,63\%=88,37\%\end{matrix}\right.\)
b) Theo PT (2): \(n_{O_2}=\dfrac{1}{2}n_{KMnO_4\left(p\text{ư}\right)}+\dfrac{3}{2}n_{KClO_3}\)
\(\Rightarrow n_{KMnO_4\left(p\text{ư}\right)}=2.\left(0,048-\dfrac{3}{2}.0,012\right)=0,06\left(mol\right)\)
\(n_{KMnO_4\left(b\text{đ}\right)}=\dfrac{12,536-0,012.122,5}{158}=0,07\left(mol\right)\)
\(\Rightarrow n_{KMnO_4\left(d\text{ư}\right)}=0,07-0,06=0,01\left(mol\right)\)
\(n_{KCl}=\dfrac{74,5}{74,5}+0,012=1,012\left(mol\right)\)
Theo PT (1): \(n_{K_2MnO_4}=n_{MnO_2}=\dfrac{1}{2}.n_{KMnO_4\left(p\text{ư}\right)}=0,03\left(mol\right)\)
PTHH:
\(2KMnO_4+10KCl+8H_2SO_4\rightarrow6K_2SO_4+2MnSO_4+5Cl_2+8H_2O\) (4)
\(K_2MnO_4+4KCl+4H_2SO_4\rightarrow3K_2SO_4+MnSO_4+2Cl_2+4H_2O\) (5)
\(MnO_2+2KCl+2H_2SO_4\rightarrow MnSO_4+K_2SO_4+Cl_2+2H_2O\) (6)
\(2KCl+H_2SO_4\xrightarrow[]{t^o}K_2SO_4+2HCl\) (7)
Theo PT (4), (5), (6): \(n_{KCl\left(p\text{ư}\right)}=5n_{KMnO_4\left(d\text{ư}\right)}+4n_{K_2MnO_4}+2n_{MnO_2}=0,23\left(mol\right)< 1,012\left(mol\right)=n_{KCl\left(b\text{đ}\right)}\)
`=> KCl` dư
Theo PT (4), (5), (6): \(n_{Cl_2}=\dfrac{1}{2}.n_{KCl\left(p\text{ư}\right)}=0,115\left(mol\right)\)
\(\Rightarrow V_{kh\text{í}}=V_{Cl_2}=0,115.22,4=2,576\left(l\right)\)

a. Ag không phản ứng nên ta có PTHH: \(2Mg+O_2\rightarrow^{t^o}2MgO\)
\(\rightarrow m_{O_2}=m_{hh}-m_{\mu\text{ối}}=18,8-15,6=3,2g\)
\(\rightarrow n_{O_2}=\frac{3,2}{32}=0,1mol\)
b. \(\rightarrow V_{O_2}=n.22,4=22,4.0,1=2,24l\)
\(\rightarrow V_{kk}=4,48.5=11,2l\)
c. Có \(n_{Mg}=2n_{O_2}=0,2l\)
\(\rightarrow m_{Mg}=0,2.24=4,8g\)
\(\rightarrow\%m_{Mg}=\frac{4,8.100}{15,6}\approx30,77\%\)
\(\rightarrow\%m_{Ag}=100\%-30,77\%=69,23\%\)

Y gồm CO ( a mol ) và CO2 (b mol )
Có a + b = nY = 0,04 (1)
MY = 16.2 = 32 ⇒ 32(a + b) = 28a + 44b (2)
Từ (1) và (2) ⇒ a = 0,03 ; b= 0,01
Bảo toàn nguyên tố O⇒ nO2 = ( a + 2b )/2 = 0,025
2KClO3 → 2KCl + 3O2
x 3x/2
2KMnO4 → K2MnO4 + MnO2 + O2
y y/2
Có hệ :
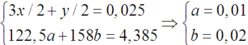
⇒ %mKMnO4 = 158×0,02 : 4,385 = 72,06%
Đáp án B

Gọi số mol MgCO3, CaCO3 là a, b (mol)
=> 84a + 100b = 1,84 (1)
PTHH: MgCO3 --to--> MgO + CO2
a-------------------->a
CaCO3 --to--> CaO + CO2
b-------------------->b
=> a + b = \(\dfrac{0,448}{22,4}=0,02\) (2)
(1)(2) => a = 0,01 (mol); b = 0,01 (mol)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,01.84}{1,84}.100\%=45,65\%\\\%m_{CaCO_3}=\dfrac{0,01.100}{1,84}.100\%=54,35\%\end{matrix}\right.\)

\(n_{Al}=\dfrac{1,728}{27}=0,064\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
____0,064->0,048
=> mO2 = 0,048.32 = 1,536 (g)
\(m_B=\dfrac{0,894.100}{8,127}=11\left(g\right)\)
Theo ĐLBTKL: mA = mB + mO2
=> mA = 11 + 1,536 = 12,536 (g)
a, \(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)gdf
b, Gọi số mol KClO3 và KMnO4 lần lượt là x,y ( mol ) ( x,y > 0 )
\(2KClO_3\underrightarrow{t^0}2KCl+3O_2\)
x(mol)......................\(\dfrac{3}{2}x\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
y(mol)..............................................\(\dfrac{1}{2}y\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Tổng số mol O2 : \(\dfrac{3}{2}x+\dfrac{1}{2}y=0,05\left(1\right)\)
\(m_{KClO_3}=n.M=122,5x\left(g\right)\)
\(m_{KMnO_4}=n.M=158y\left(g\right)\)
\(\Rightarrow122,5x+158y=8,77\left(2\right)\)
Từ (1)(2) ,có :\(\left\{{}\begin{matrix}\dfrac{3}{2}x+\dfrac{1}{2}y=0,05\\122,5x+158y=8,77\end{matrix}\right.\) ( bấm máy tính là ra )
\(\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,04\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{KClO_3}=122,5.x=122,5.0,02=2,45\left(g\right)\\m_{KMnO_4}=158y=158.0,04=6,32\left(g\right)\end{matrix}\right.\)
\(\%m_{KClO_3}=\dfrac{2,45}{8,77}.100\%=27\%\)
\(\%m_{KMnO_4}=\dfrac{6,32}{8,77}.100\%=73\%\)
nO2=1,12/22,4=0,05(mol)
2KClO3--->2KCl+3O2
x_______________3/2x
2KMnO4--->K2MnO4+MnO2+O2
y__________________________1/2y
Hệ pt:
\(\left\{{}\begin{matrix}122,5x+158y=8,77\\1,5x+0,5y=0,05\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,02\\y=0,04\end{matrix}\right.\)
=>mKClO3=0,02.122,5=2,45(g)
=>%mKClO3=2,45/8,77.100%~27,9%
=>%mKMnO4=100%-27,9%=72,1%